
【题目】随着科技进步和人类环保意识的增强,如何利用CO2已经成为世界各国特别关注的问题。
已知:CO2与CH4经催化重整制得合成气:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g) △H
2CO(g)+2H2(g) △H
(1)降低温度,该反应速率会_______________(填“增大”或“减小”);一定压强下,由最稳定单质生1 mol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395 kJ/mol、-74.9 kJ/mol、-110.4 kJ/mol。则上述重整反应的ΔH=____________kJ/mol。
(2)T1℃时,在两个相同刚性密闭容器中充入CH4和CO2分压均为20 kPa,加入催化剂Ni/α-Al2O3并分别在T1℃和T2℃进行反应,测得CH4转化率随时间变化如图Ⅰ所示。
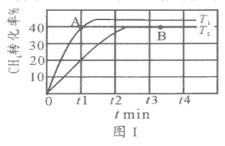
①A点处v正_______B点处(填“<”、“>”或“=”)
②研究表明CO的生成速率v生成(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,A点处v生成(CO)=__________mol·g-1·s-1。
(3)上述反应达到平衡后,若改变某一条件,下列变化能说明平衡一定正向移动的是________________(填代号)。
A.正反应速率增大 B.生成物的百分含量增大 C.平衡常数K增大
(4)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图Ⅱ,C点___________________(填“可能”、“一定”或“一定未”)达到平衡状态,理由是_____________;CH4的转化率b点高于a点的可能原因是_________________________________。
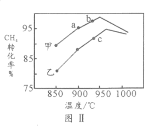
【答案】减小 +249.1 > 1.872 C 一定未 催化剂不会改变平衡转化率,乙催化剂c点未与甲催化剂同样温度的点相交,转化率不相等,说明c点不是平衡转化率 b和a两点反应都未达平衡,b点温度高,反应速率快,相同时间内转化率高(或其它合理答案)
【解析】
(1)降低温度,降低反应混合物中分子所具有的能量;
反应焓变△H=生成物的反应焓之和-反应物的反应焓之和;
(2)①根据图Ⅰ,T1的温度高于T2,速率大;
②由图,A点甲烷的转化率为40%,算出分压,代入公式计算;
(3)A.正反应速率增大,如逆速率同等程度地增加,平衡不移动;
B.向反应体系中投入某生成物,生成物的百分含量增大,但平衡逆向移动;
C.平衡常数K增大,平衡正向进行的程度增大;
(4)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图Ⅱ,C点一定未达到平衡状态,理由是催化剂不会改变平衡转化率,乙催化剂c点未与甲催化剂同样温度的点相交,转化率不相等,说明c点不是平衡转化率;
CH4的转化率b点高于a点的可能原因是:b和a两点反应都未达平衡,b点温度高,反应速率快,相同时间内转化率高(或其它合理答案)。
(1)降低温度,降低反应混合物中分子所具有的能量,该反应速率会减小;
CH 4(g)与CO 2(g)反应生成CO(g)和H 2(g)的方程式:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395 kJ/mol、-74.9 kJ/mol、-110.4 kJ/mol。根据此定义,稳定单质的摩尔生成焓为0,反应焓变△H=2×(-110.4KJ·mol-1)-[(-395KJ·mol-1)+(-74.9KJ·mol-1)]=+249.1kJ·mol-1,反应的热化学方程式为:CH4(g)+CO2(g)
2CO(g)+2H2(g),CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395 kJ/mol、-74.9 kJ/mol、-110.4 kJ/mol。根据此定义,稳定单质的摩尔生成焓为0,反应焓变△H=2×(-110.4KJ·mol-1)-[(-395KJ·mol-1)+(-74.9KJ·mol-1)]=+249.1kJ·mol-1,反应的热化学方程式为:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)△H=+249.1kJ·mol-1。
2CO(g)+2H2(g)△H=+249.1kJ·mol-1。
(2)①根据图Ⅰ,T1的温度高于T2,A点处v正>B点处;
②由图,A点甲烷的转化率为40%,结合方程式CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),p(CH4)=20KPa×(1-40%)=12kPa=p(CO2),CO的生成速率v生成(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,A点处v生成(CO)=1.3×10-2×12×12mol·g-1·s-1=1.872mol·g-1·s-1。
2CO(g)+2H2(g),p(CH4)=20KPa×(1-40%)=12kPa=p(CO2),CO的生成速率v生成(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,A点处v生成(CO)=1.3×10-2×12×12mol·g-1·s-1=1.872mol·g-1·s-1。
(3)A.正反应速率增大,如逆速率同等程度地增加,平衡不移动,故A不符;
B.向反应体系中投入某生成物,生成物的百分含量增大,但平衡逆向移动,故B不符;
C.平衡常数K增大,平衡正向进行的程度增大,故C符合;
故选C。
(4)其他条件相同,在甲、乙两种不同催化剂作用下,相同时间内测得CH4转化率与温度变化关系如图Ⅱ,C点一定未达到平衡状态,理由是催化剂不会改变平衡转化率,乙催化剂c点未与甲催化剂同样温度的点相交,转化率不相等,说明c点不是平衡转化率;
CH4的转化率b点高于a点的可能原因是:b和a两点反应都未达平衡,b点温度高,反应速率快,相同时间内转化率高(或其它合理答案)。


科目:高中化学 来源: 题型:
【题目】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是

A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室用重晶石(主要成分BaSO4)对工业生产BaS进行模拟实验。BaS是可溶盐,在工业生产中,它是制备其他钡盐的中间产物。已知:
BaSO4(s)+4C(s)![]() 4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1 ①
4CO(g)+BaS(s) ΔH1=+571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)![]() 2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
2CO2(g)+BaS(s) ΔH2=+226.2 kJ·mol-1 ②
下列说法不正确的是( )
A.上述反应中BaSO4均作氧化剂
B.反应C(g)+CO2(g)![]() 2CO(g)的ΔH3>+172.5 kJ·mol-1
2CO(g)的ΔH3>+172.5 kJ·mol-1
C.实际生产中必须加入过量的炭使BaSO4得到充分的还原,同时还要通入空气,因为①②为吸热反应,炭和氧气反应放热维持反应所需高温
D.以BaS作为沉淀剂,用于铅和汞沉淀的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰(CN)2,硫氰(SCN)2等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: Cl-<Br-<CN-<SCN-<I-,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是
A.4HCN(浓)+MnO2![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
B.(CN)2+H2O=2H++CN-+CNO-
C.(CN)2+2OH-=CN-+CNO-+H2O
D.(CN)2+2SCN-=2CN-+(SCN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯是一种有水果香味的油状液体,实验室通常用乙酸与乙醇在浓硫酸存在并加热的条件下反应生成乙酸乙酯。请回答:
(1)工业上常用乙烯水化法制备乙醇,乙烯的结构简式为____________。
(2)制备乙酸乙酯的化学方程式为__________________________,该反应的类型是_______反应。
(3)乙醇俗称酒精,是一种重要无污染的燃料和化工原料,乙醇的官能团为__________(写名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 则
则![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下反应均可生成![]() 。下列有关说法正确的是
。下列有关说法正确的是![]()
![]() 二氧化碳分解生成氧气:
二氧化碳分解生成氧气:![]() ;
;![]()
![]() 过氧化氢分解生成氧气:
过氧化氢分解生成氧气:![]() ;
;![]()
![]() 光照条件下,催化分解水蒸气生成氧气:
光照条件下,催化分解水蒸气生成氧气:![]() ;
;![]() 。
。
A.反应![]() 使用催化剂,能降低该反应的活化能
使用催化剂,能降低该反应的活化能
B.反应![]() 为吸热反应
为吸热反应
C.反应![]() 将化学能转化为光能
将化学能转化为光能
D.反应![]() ;
;![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法错误的是( )
A.CH3OH转变成H2的反应不一定要吸收能量
B.1mol CH3OH(g)完全燃烧放出的热量大于192.9 kJ
C.反应①中的能量变化如图所示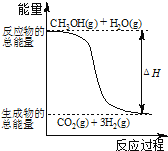
D.根据反应①和②推知:H2(g)+1/2O2(g)=H2O(g) ΔH=-241.9kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】面对世界范围内的能源危机,甲醇作为一种可再生能源,有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:____
(2)对于CO(g)+2H2(g)CH3OH(g) ΔH1=-90 kJ·mol-1,在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时CO的转化率与温度、压强的关系如图所示。
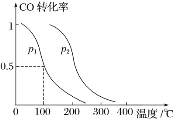
①p1 _______(填“大于”“小于”或“等于”) p2。
②在其他条件不变的情况下,缩小体积使压强增大,达到新平衡时,CO的转化率________(填“增大”“减小”或“不变”),平衡常数________(填“增大”“减小”或“不变”)。
(3)已知在温度T时,CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1 mol·L-1,c始(H2O)=1 mol·L-1,某时刻经测定CO的转化率为10%,判断此时刻υ正________(填“>” 、“=”或“<”)υ逆。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com