
【题目】生产自来水最重要的两步工序是净化和消毒,净化一般使用![]() ,消毒一般使用
,消毒一般使用![]() 。
。
(1)![]() 溶液呈酸性的原因是(用离子方程式表示)____________;
溶液呈酸性的原因是(用离子方程式表示)____________;![]() 具有净水作用,但会腐蚀钢铁设备,除
具有净水作用,但会腐蚀钢铁设备,除![]() 作用外,另一主要原因是(用离子方程式表示):____________。
作用外,另一主要原因是(用离子方程式表示):____________。
(2)氯气的水溶液称为氯水,氯水中存在多个平衡,写出其中两个含氯元素的平衡方程式:____________、____________。氯水中存在![]() 分子、
分子、![]() 分子和
分子和![]() 分子,不存在
分子,不存在![]() 分子的原因是_______,除水分子外,新制氯水中含量最多的微粒是__________。
分子的原因是_______,除水分子外,新制氯水中含量最多的微粒是__________。
(3)次氯酸有漂白杀菌作用,其作用原理是![]() ,该变化是____________反应(选填“氧化”、“还原”、“氧化还原”);在
,该变化是____________反应(选填“氧化”、“还原”、“氧化还原”);在![]() 溶液中通入少量
溶液中通入少量![]() 气体,只发生如下反应:
气体,只发生如下反应:![]() ,由此判断
,由此判断![]() 、
、![]() 和
和![]() 的酸性由强到弱的顺序是____________。
的酸性由强到弱的顺序是____________。
(4)![]() 能用于自来水消毒,还能除去水中的
能用于自来水消毒,还能除去水中的![]() 杂质,产物为
杂质,产物为![]() 和盐酸。写出该反应的离子方程式__________________。
和盐酸。写出该反应的离子方程式__________________。
【答案】![]()
![]()
![]()
![]()
![]() 是强电解质,在水中完全电离
是强电解质,在水中完全电离 ![]() 还原
还原 ![]()
![]()
【解析】
(1)![]() 是强酸弱碱盐,在水溶液中易发生水解而使溶液呈酸性,离子方程式为
是强酸弱碱盐,在水溶液中易发生水解而使溶液呈酸性,离子方程式为![]() 。
。![]() 会腐蚀钢铁设备,除
会腐蚀钢铁设备,除![]() 作用外,另一主要原因为
作用外,另一主要原因为![]() ;
;
(2)氯水中存在多个平衡,其中两个含氯元素的平衡方程式为:![]() ,
,![]() 。氯水中不存在
。氯水中不存在![]() 分子的原因是
分子的原因是![]() 是强电解质,在水中完全电离。除水分子外,新制氯水中含量最多的微粒是
是强电解质,在水中完全电离。除水分子外,新制氯水中含量最多的微粒是![]() 。 (3)次氯酸有漂白杀菌作用,其作用原理是
。 (3)次氯酸有漂白杀菌作用,其作用原理是![]() ,在该变化中,只有Cl由+1价降低到-1价,所以该反应是还原反应。在
,在该变化中,只有Cl由+1价降低到-1价,所以该反应是还原反应。在![]() 溶液中通入少量
溶液中通入少量![]() 气体,只发生如下反应:
气体,只发生如下反应:![]() 。根据强酸制备弱酸的原理可知
。根据强酸制备弱酸的原理可知![]() 、
、![]() 和
和![]() 的酸性由强到弱的顺序是
的酸性由强到弱的顺序是![]() ;
;
(4)![]() 能用于自来水消毒,还能除去水中的
能用于自来水消毒,还能除去水中的![]() 杂质,产物为
杂质,产物为![]() 和盐酸。该反应的离子方程式
和盐酸。该反应的离子方程式![]() 。
。


科目:高中化学 来源: 题型:
【题目】由甲酸甲酯、葡萄糖、乙醛、丙酸四种物质组成的混合物,已知其中氧元素的质量分数为44%,则氢元素的质量分数为( )
A. 48%B. 8%C. 56%D. 10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列各题。
(1)将2molL-1Al2(SO4)3和0.2molL-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=___molL-1.若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2molL-1稀硫酸,计算需要量取___mL的浓硫酸。(读到小数点后一位)
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g。此混合物中CO和CO2分子数目之比是___,混合气体的平均摩尔质量是___。
(3)还原铁粉与高温水蒸气反应的化学方程式:___。
(4)除去Mg粉中的Al粉的试剂是___,反应的离子方程式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铝浸入![]() 溶液中,取出晾干,置于空气中,表面会生成毛状物质(俗称毛刷),反应为4Al(Hg)+3O2+2xH2O→2(Al2O3xH2O),下列说法正确的是( )
溶液中,取出晾干,置于空气中,表面会生成毛状物质(俗称毛刷),反应为4Al(Hg)+3O2+2xH2O→2(Al2O3xH2O),下列说法正确的是( )
A.![]() 发生氧化反应,
发生氧化反应,![]() 是氧化剂
是氧化剂
B.![]() 既是氧化产物也是还原产物
既是氧化产物也是还原产物
C.该反应属于置换反应
D.当![]() 铝参加反应,转移电子数为
铝参加反应,转移电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
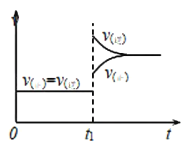
【题目】对于反应![]() ,减小压强,平衡向______(填“正反应”或“逆反应”)方向移动,平衡混合气体的平均相对分子质量在平衡移动时______(填“是”或“否”)发生改变,其原因是____________;下图是反应速率与时间的关系图,
,减小压强,平衡向______(填“正反应”或“逆反应”)方向移动,平衡混合气体的平均相对分子质量在平衡移动时______(填“是”或“否”)发生改变,其原因是____________;下图是反应速率与时间的关系图,![]() 时刻引起正、逆反应速率变化的原因可能是____________(写一条合理原因)。
时刻引起正、逆反应速率变化的原因可能是____________(写一条合理原因)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 mol甲烷与一定量的氯气混合于一量筒中,倒立于盛有饱和食盐水的水槽(如图所示),对于此反应,有关叙述不正确的是( )
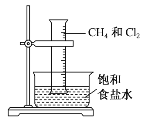
A.该反应的生成物只有四种
B.该反应的条件是光照
C.该反应属于取代反应
D.该反应现象有量筒内气体颜色变浅,器壁上有油状液滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保水剂是一种强吸水树脂,能在短时间内吸收自身重量几百倍至上千倍的水分。聚丙烯酸钠就是一种高吸水性树脂。下面是丙烯合成聚丙烯酸钠的化工流程:

(1)上述反应中属于加成反应的有____________,反应⑧的反应类型为____________;
(2)若(1)的反应条件为通过溴的四氯化碳溶液,请写出A的结构简式____________;D中官能团名称是____________。
(3)请写出C→D的化学反应方程式__________________。
(4)![]() 是
是![]() 的同系物,式量比
的同系物,式量比![]() 大14,写出2种符合下列要求的
大14,写出2种符合下列要求的![]() 的同分异构体:①链状分子;②与新制氢氧化铜在加热条件下反应生成砖红色沉淀;③与
的同分异构体:①链状分子;②与新制氢氧化铜在加热条件下反应生成砖红色沉淀;③与![]() 溶液混合后滴入酚酞,加热,溶液颜色变浅。__________、___________
溶液混合后滴入酚酞,加热,溶液颜色变浅。__________、___________
(5)检验反应(4)是否全部转化的实验方案__________________。
(6)丙酮(![]() )是一种常用的化工试剂,请设计一条由丙烯制备丙酮的合成路线。(合成路线常用的表示方式为:
)是一种常用的化工试剂,请设计一条由丙烯制备丙酮的合成路线。(合成路线常用的表示方式为:![]() )
)
____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料G的一种合成工艺如图所示。
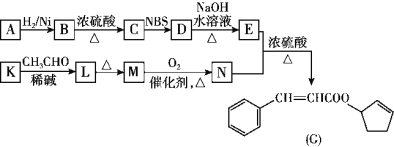
核磁共振氢谱显示A有两组峰,其强度之比为1∶1。
已知:(1)CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
(2)CH3CHO+CH3CHO![]()
![]()
![]() CH3CH=CHCHO+H2O
CH3CH=CHCHO+H2O
请回答下列问题:
(1)A的结构简式为____________,G中官能团的名称为____________________。
(2)检验M已完全转化为N的实验操作是__________________。
(3)有学生建议,将M→N的转化用KMnO4(H+)代替O2,老师认为不合理,原因是_______________。
(4)写出K→L的化学方程式:____________________,反应类型为________。
(5)F是比M多一个碳原子的同系物,满足下列条件的F的同分异构体有________种(不考虑立体异构)。
①能发生银镜反应
②能与溴的四氯化碳溶液加成
③苯环上有2个对位取代基
(6)以丙烯和NBS试剂为原料制备甘油(丙三醇),请设计合成路线(其他无机原料任选) _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.1。反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
COS(g)+H2(g) K=0.1。反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是( )
A. 平衡后若升高温度,H2S浓度增加,表明该反应是吸热反应
B. 当体系的压强保持不变时,表明该反应达到化学平衡状态
C. CO的平衡转化率为80%
D. 反应前H2S物质的量为7mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com