
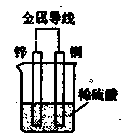
| A.电流从锌电极经金属导线流向铜电极 |
| B.锌为阴极,铜为阳极 |
| C.负极的电极反应式为:Zn—2e→Zn2+ |
| D.一段时间后,溶液中阳离子浓度增大、阴离子浓度不变 |
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源:不详 题型:单选题
| A.构成原电池正极和负极的材料必须是两种金属? |
| B.由Cu、Zn作电极与CuSO4溶液组成的原电池中,Cu上产生气泡? |
| C.氢氧燃料电池中,把H2通入正极,此极发生氧化反应 |
| D.在锌铜原电池外电路中,电子由锌流向铜 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.废旧电池应集中回收,并填埋处理 |
| B.锌锰干电池工作一段时间后碳棒变细 |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
| D.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
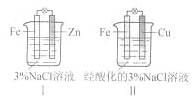
| A.Ⅰ是验证牺牲阳极的阴极保护法的实验装置 |
| B.Ⅰ和Ⅱ中负极反应均是Fe-2e-=Fe2+ |
| C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-=4OH- |
| D.Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
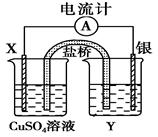
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌为负极,空气进入负极发生反应 |
| B.正极发生氧化反应,负极发生还原反应 |
| C.负极电极反应是:Zn – 2e- +2OH-=ZnO+H2O |
| D.电池工作时,溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
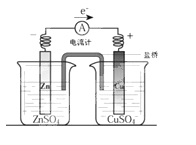
| A.铜是阳极,铜片上有气泡产生 |
| B.铜离子在铜片表面被还原 |
| C.电流从锌片经导线流向铜片 |
| D.正极附近的SO42-离子浓度逐渐增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Ag+Zn(OH)2,在此电池放电时,负极上发生反应的物质是( )
2Ag+Zn(OH)2,在此电池放电时,负极上发生反应的物质是( )| A.Zn(OH)2 | B.Ag | C.Ag2O | D.Zn |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 浓度均为0.4 mol·L-1
浓度均为0.4 mol·L-1 ,工作一段时间后,测得导线上均通过了0.10mol电子,此时溶液中的pH由大到小的顺序是]
,工作一段时间后,测得导线上均通过了0.10mol电子,此时溶液中的pH由大到小的顺序是]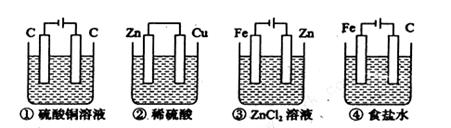
| A.①②③④ | B.②①③④ | C.③①②④ | D.④③①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com