
 2Ag+Zn(OH)2,在此电池放电时,负极上发生反应的物质是( )
2Ag+Zn(OH)2,在此电池放电时,负极上发生反应的物质是( )| A.Zn(OH)2 | B.Ag | C.Ag2O | D.Zn |
科目:高中化学 来源:不详 题型:单选题
| A.C2H5OH在电池的负极上参加反应 |
| B.1mol乙醇被氧化转移6mol电子 |
| C.在外电路中电子由负极沿导线流向正极 |
| D.电解质溶液中阳离子移向正极,阴离子移向负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
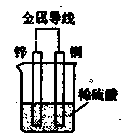
| A.电流从锌电极经金属导线流向铜电极 |
| B.锌为阴极,铜为阳极 |
| C.负极的电极反应式为:Zn—2e→Zn2+ |
| D.一段时间后,溶液中阳离子浓度增大、阴离子浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜锌原电池中铜是正极 |
| B.用电解法精炼粗铜时用纯铜作阳极 |
| C.在镀件上电镀铜时镀件不作阴极 |
| D.电解稀硫酸制H2、O2时铜与电源正极相连 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 的顺序是________。
的顺序是________。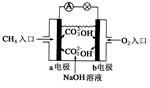
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
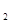 溶液、Fe
溶液、Fe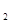 (SO
(SO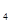 )
) 溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。
溶液、盐酸。按要求回答下列问题:若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池? (填“能”或“不能”)。若能,请写出电极反应式:负极 ,正极 。若不能,请说明原因 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.通入O2的电极为负极 |
| B.正极反应式为:O2+4e-+2H2O=4OH- |
| C.电池工作时H+移向负极 |
| D.负极反应式为:2SO2 - 4e- + 4H2O = 2SO42- + 8H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钢板中的铁做负极,电极反应为Fe — 2e- ="=" Fe2+ |
| B.放电时正极上有氧气生成 |
| C.放电时OH-向正极移动 |
| D.电池总反应为:2Li+2H2O="==" 2LiOH+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com