
| A. | (△H2-△H3 ):2(△H1-△H3) | B. | (△H3-△H2 ):($\frac{△{H}_{1}}{2}$-△H3) | ||
| C. | (△H3-△H2 ):(△H3-$\frac{△{H}_{1}}{2}$) | D. | ($\frac{△{H}_{1}}{2}$-△H2 ):(△H3-△H2) |
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①③⑤ | C. | ②④⑤⑥ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3用作耐火材料、Al(OH)3用作阻燃剂 | |
| B. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| C. | 碳素钢的主要成分是铁碳合金、司母戊鼎的主要成分是铜锡合金 | |
| D. | 盛放NaOH溶液的磨口玻璃瓶要用橡胶塞 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
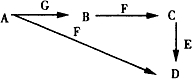 A~G为中学化学中常见的物质,B、E、F为单质,在常温下B是一种有色气体,G为黑色的固体.它们的相互转化如图所示,部分生成物未列出.试回答下列问题
A~G为中学化学中常见的物质,B、E、F为单质,在常温下B是一种有色气体,G为黑色的固体.它们的相互转化如图所示,部分生成物未列出.试回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 氢气在氯气中燃烧:H2+Cl2═2H++2Cl- | |
| C. | 小苏打治疗胃酸过多:H++HCO3-═H2O+CO2↑ | |
| D. | 用氯化铁溶液腐蚀铜箔制造印刷电路板:Fe3++Cu═Fe2++Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com