
����Ŀ���������㷺�ֲ���ֲ����漰�������ڣ��Ƕ������Ϻ�ҩ�����Ҫ�ɷ֡�I��һ�����������ĺϳ�·�����£�


�ش��������⣺
(1)�������ŷ��࣬A�������______��
(2)A��C�ķ�Ӧ������______��
(3)C��D��E��F�Ļ�ѧ����ʽ�ֱ���______��______��
(4)д���������ʵĽṹ��ʽ��B______��H______��
(5)F��G�ķ�Ӧ�У�������������______��
(6)ʮ������ĩO.Wallach���ֲ�������������ϩ������������Ȼ���д��ڵ������������Կ����������ϩ�ľۺ���������Ϊ���������������Ŀ������о���1910�걻����ŵ������ѧ��������CH3CH2OH��CH3MgI��CH3CH2MgBrΪ�л�ԭ�ϣ������Ŀ������Ϣ��ѡ�ñ�Ҫ�����Լ�����ȫ�����ϩ(![]() )�ĺϳ�·��____________________��
)�ĺϳ�·��____________________��

���𰸡��� ȡ����Ӧ  E��F
E��F

 �������ǻ���������
�������ǻ��������� 
��������
�ɷ�Ӧ������D�Ľṹ��ʽΪ ��֪��CΪ
��֪��CΪ �������Ϣ����֪��BΪ
�������Ϣ����֪��BΪ ������Ϣ��������֪��EΪ
������Ϣ��������֪��EΪ ���ɷ�Ӧ������I�Ľṹ��ʽ
���ɷ�Ӧ������I�Ľṹ��ʽ ��֪��HΪ
��֪��HΪ ���ɷ�Ӧ������֪GΪ
���ɷ�Ӧ������֪GΪ ��
��
��1��A�����к��з��ǻ������ڷ��࣬���ַӵ����ʣ��ʴ�Ϊ���ӣ�
��2��A��C�ķ�ӦΪ![]() ��
�� ����ȡ����Ӧ����
����ȡ����Ӧ���� ���ʴ�Ϊ��ȡ����Ӧ��
���ʴ�Ϊ��ȡ����Ӧ��
��3��C��D�ķ�ӦΪ��Ũ���������£� ��״����ȷ���������Ӧ����
��״����ȷ���������Ӧ���� ��ˮ����Ӧ�Ļ�ѧ����ʽΪ
��ˮ����Ӧ�Ļ�ѧ����ʽΪ ��E��F�ķ�ӦΪ
��E��F�ķ�ӦΪ ��Ũ���������£�������������ˮ��Ӧ����
��Ũ���������£�������������ˮ��Ӧ���� ����Ӧ�Ļ�ѧ����ʽΪ
����Ӧ�Ļ�ѧ����ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
��
��4��������ͼ��֪��BΪ ��HΪ
��HΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
�� ��
��
��5��F��G�ķ�Ӧ�У������������� ����ȥ��Ӧ����
����ȥ��Ӧ���� ��
�� �����Ը����������Ϊ
�����Ը����������Ϊ ��
�� ˮ������
ˮ������ ��˵��F��G�ķ�Ӧ�У��������������DZ������ǻ������������ʴ�Ϊ���������ǻ�����������
��˵��F��G�ķ�Ӧ�У��������������DZ������ǻ������������ʴ�Ϊ���������ǻ�����������
��6���������Ӧ�����Ϣ��֪��![]() Ӧ�ȱ�����Ϊ
Ӧ�ȱ�����Ϊ![]() ��
��![]() ������Ϣ����Ӧ����
������Ϣ����Ӧ���� ��
�� ��Ũ���������·�����ȥ��Ӧ����
��Ũ���������·�����ȥ��Ӧ����![]() ��
��![]() ��������Ȼ�̼��Һ�����ӳɷ�Ӧ����
��������Ȼ�̼��Һ�����ӳɷ�Ӧ���� ��
�� ���������ƴ���Һ�м��ȷ�ʽ��ȥ��Ӧ����
���������ƴ���Һ�м��ȷ�ʽ��ȥ��Ӧ����![]() ���ϳ�·�����£�
���ϳ�·�����£� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Դ���ճ�����߿Ƽ������ж��й㷺Ӧ�á�

����ͼ�ҡ�������������ص��ܵ缫��Ӧ����ʽ���£�
ͼ�ң�Zn+Ag2O+H2O�TZn��OH��2+2Ag
ͼ����Zn+2NH4Cl+2MnO2�TZn��NH3��2Cl2+MnO��OH��
ͼ����PbO2+Pb+2H2SO4�T2PbSO4+2H2O
����˵������ȷ���ǣ�������
A. �ף�Zn2+��Cu�缫�����ƶ���Cu�缫������Һ��H+Ũ������
B. �ң������ĵ缫��ӦʽΪAg2O+2e��+H2O�T2Ag+2OH��
C. ����пͲ������������������Ӧ��пͲ��䱡
D. ����ʹ��һ��ʱ��������Һ�����Լ��������������½�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̽�����ʵ�صĹ���ԭ��ʱ��ij����С��ͬѧ���֣�����ͼ����ʾ����һ������ʱ�������ܲ����⣻��ͼ����ʾ���Ӽ�������ʱ�������ܷ��⡣����˵������ȷ����

A. ͼ���ж����ܲ����⣬˵����װ�ò�����ԭ���
B. ͼ��������Ϊ������ͭ��Ϊ�����������ĵ缫��ӦΪ��Fe��2 e��===Fe2+
C. ͼ���ж����ܲ������ԭ���ǵ������ʵ�صĵ�ѹ��С
D. ͼ�������õĵ������ܵ�ѹ�Ǹ������ʵ�صĵ�ѹ֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1g���ȼ���£�N2H4������ȼ������N2��H2O��g��ʱ���ų�16.7kJ����������÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����
A. N2H4+O2=N2+2H2O ��H=��534.4kJ/mol
B. N2H4��g��+O2(g)=N2(g)+2H2O(g) ��H=��534.4kJ/mol
C. N2H4��g��+O2(g)=N2(g)+2H2O(g) ��H= +534.4kJ/mol
D. ![]() N2H4��g��+
N2H4��g��+![]() O2(g)=
O2(g)=![]() N2(g)+H2O(g) ��H=��16.7kJ/mol
N2(g)+H2O(g) ��H=��16.7kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������(NH4)2Fe(SO4)26H2O�ֳ�Ī���Σ���dz��ɫ���塣��������(��Ҫ��FeS2��SiO2��)�Ʊ�Ī���ε��������£�

��֪��FeS2��H2SO4����Ӧ����Ӧ���ʵ��ܽ����������ͼ��
(1)FeS2��SԪ�صĻ��ϼ�Ϊ______��
(2)�������յ�����Ӧ�ǣ�4FeS2+11O2![]() 2Fe2O3+8SO2���ӿ������������ʵĴ�ʩ��______(д���㼴��)��
2Fe2O3+8SO2���ӿ������������ʵĴ�ʩ��______(д���㼴��)��
(3)��H2SO4�����������Ӧ�����ӷ���ʽΪ______��
(4)����ԭ��ʱ��Fe3+��ͨ����Ӧ������FeS2��ԭ����Ӧ��Ϊ��FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42��+16H+��Ӧ������ӷ���ʽΪ��______��
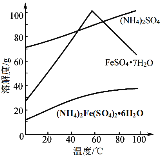
(5)�õ�Ī���ξ���IJ����ǣ�����Ũ�����ᾧ�����ˡ�ϴ�ӡ��ᾧ������ʱѡ��������¶�Ϊ60�棬����ѡ����¶ȵ�ԭ��______��
(6)Ϊ֤������Ī���ξ����к���Fe2+��NH4+��ʵ�鷽����ȡ��������Һ��һ֧�Թ�����______��֤������Fe2+��NH4+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʳ��ˮ��ȡClO2�Ĺ�ҵ������ͼ��ʾ��װ�â��еķ�Ӧ��NaCl+3H2O![]() NaClO3+3H2����װ�â��еķ�Ӧ��2NaClO3+4HCl
NaClO3+3H2����װ�â��еķ�Ӧ��2NaClO3+4HCl![]() 2ClO2+ Cl2��+2NaCl+2H2O�����й��ڸ�����˵������ȷ���ǣ� ��
2ClO2+ Cl2��+2NaCl+2H2O�����й��ڸ�����˵������ȷ���ǣ� ��

A. ��������Cl2��NaCl������ѭ������
B. װ�â���H2����������
C. װ�âڷ����ķ�Ӧ�У�Cl2���������NaCl�ǻ�ԭ����
D. Ϊ��ʹH2��ȫת��ΪHCl����Ҫ��װ�â��в���Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦNH2COONH4(s) ![]() 2NH3(g)+CO2(g),�������������Կ϶��÷�Ӧ�ﵽƽ��״̬���ǡ�(����)
2NH3(g)+CO2(g),�������������Կ϶��÷�Ӧ�ﵽƽ��״̬���ǡ�(����)
A.�ܱ������а����������������B.c(NH3)��c(CO2)=2��1
C.�ܱ������е�ѹǿ����D.v(NH3)��v(CO2)=2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����������ʵ�鷽������̽��ij��Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ��

����һ����ͼ1����С�ձ����һЩ��ȥ����������Ĥ����Ƭ��Ȼ�����ձ������10 mL 2 mol/Lϡ���ᣬ�ٲ���һ֧�¶ȼƣ��¶ȼƵ��¶���20 ��������75 �棬����¶����½�������ͣ����20 �档
����������ͼ2�����ձ��ײ������ڵ�����ճһ��СľƬ�����ձ������10 mL 2 mol/L������Һ���������м�������������Һ��Ƭ�̺������ձ�������СľƬ����������
����������ͼ3�����Թ��з���ij��ѧ��Ӧ��ʵ��ǰU�ιܺ�īˮҺ����ƽ���ڻ�ѧ��Ӧ�����У�ͨ��U�ι������īˮҺ��ߵ��ж�ij��Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ��
��� | ���Թ������Ӧ������ | U�ι����īˮҺ�� |
�� | ��������ˮ | ����Ҹ� |
�� | ���������������Ȼ�茶���(��ֽ���) | �� |
�� | ��Ƭ���ռ���Һ | ����Ҹ� |
�� | ͭ��Ũ���� | ����Ҹ� |
��������ʵ��ش�������⣺
(1)����Ƭ��ϡ����ķ�Ӧ��________(��������������������)��Ӧ��
(2)�������У�СľƬ�����ԭ����_________���ɴ˵ó��Ľ�����________��
(3)�ɷ�����������ó����ۣ��٢ۢ������ʷ����ķ�Ӧ����________(��������������������)��Ӧ��
(4)������ʵ��ڵ�U�ι��е�����Ϊ___________��˵����Ӧ���������С�����������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com