
【题目】常温下,下列各组离子在指定溶液中,一定可以大量共存的是( )
A.无色溶液中??? Mg2+、Al3+、SO42﹣、CO32﹣
B.pH=1的溶液中??? NH4+、Ba2+、HCO3﹣、NO3﹣
C.含MnO4﹣的溶液中??? H+、K+、Br﹣、I﹣
D.在 ![]() =1×10﹣12的溶液中??? Na+、K+、CH3COO﹣、SO42﹣
=1×10﹣12的溶液中??? Na+、K+、CH3COO﹣、SO42﹣
科目:高中化学 来源: 题型:
【题目】A~H分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知 C为无色有刺激性气味气体,G是红褐色难溶于水的沉淀。

请填写下列空白:
(1)A的俗名是____________。C的名称是_________。
(2)从溶液 E得到H需加入___________(写出任一种物质)。
(3)反应①的离子方程式为______________________________________;
反应③的化学方程式为_____________________________________;
写出 C与溶液D反应的离子方程式:______________________________。
(4)反应③过程中的现象是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题.
(1)装置1为铁的吸氧腐蚀实验.向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 .
(2)装置2中的石墨是极(填“正”或“负”),该装置发生的总反应的离子方程式为
(3)装置3中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100mL 0.5mol/L的CuSO4溶液.反应一段时间后,停止通电.向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红.
①电源的M端为极;甲烧杯中铁电极的电极反应为 .
②乙烧杯中电解反应的离子方程式为 .
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体标准状况下体积为 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的无色水溶液只可能含有以下离子中的若干种:K+、NH4+、Fe2+、Cl-、Ca2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g.
综合上述实验,回答下列问题:
(1)不做任何实验就可以肯定原溶液中不存在的离子是__________。
(2)该混合物中一定含有的离子__________;可能含有的离子__________。
(3)K+物质的量: n(K+)_____(具体值或取值范围)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯化氢和盐酸的叙述中,正确的是( )
A. 它们都用 HCl 表示,两者没有区别
B. 氯化氢和盐酸在潮湿的空气中都形成酸雾
C. 氯化氢和盐酸都能导电
D. 氯化氢是无色气体,盐酸是无色溶液,它们都有刺激性气味
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的密闭容器中进行下列反应:C(s)+CO2(g)═2CO(g);△H=+Q kJmol﹣1 . 如图为CO2、CO的物质的量随时间t的变化关系图.下列说法不正确的是( ) 
A.在0﹣1min内CO的物质的量增加了2mol
B.当固焦炭的质量不发生变化时,说明反应已达平衡状态
C.5min时再充入一定量的CO,n(CO)、n(CO2)的变化可分别由c、b曲线表示
D.3min时温度由T1升高到T2 , 重新平衡时K(T2)小于K(T1)
查看答案和解析>>
科目:高中化学 来源: 题型:
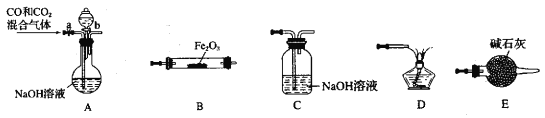
【题目】某化学兴趣小组用Fe2O3与CO反应来制取单质Fe。
(1)请按气流由左到右的方向连接下列各装置,顺序为A→____→____ →____ →____ 。___________
(2)检查装置A气密性的方法是____________________。
(3)在点燃B处的酒精灯前,应进行的操作是_______。
(4)若用100mL0.1molL的NaOH 溶液吸收224mLCO2气体(标准状况),恰好完全吸收。再将所得溶液加入100mL0.1mol/L氢氧化钙溶液中。请写出所得溶液与氢氧化钙溶液反应的离子方程式:________________。
(5)配制100mL 0.1mol/LNaOH 溶液时,下列操作会导致所配溶液浓度偏高的操作是______。A.容量瓶用蒸馏水洗涤后未进行干燥处理,底部有少量水残留。
B.用蒸馏水溶解氢氧化钠固体后,立即转移到容量瓶中,然后洗涤、定容。
C.定容摇匀后,发现液面低于刻度线,又加水到刻度线位置
D.定容时仰视刻度线
E.称量氢氧化钠固体时所用砝码生锈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g火箭燃料肼(N2H4)气体燃烧生成N2(g)和H2O(g)时,放出16.7 kJ的热量,则该反应的热化学方程式正确的是
A.N2H4+O2![]() N2+2H2O ΔH=534.4 kJ·mol1
N2+2H2O ΔH=534.4 kJ·mol1
B.N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ΔH=534.4 kJ·mol1
N2(g)+2H2O(g) ΔH=534.4 kJ·mol1
C.N2H4(g)+O2(g)![]() N2(g)+2H2O(g) ΔH=+534.4 kJ·mol1
N2(g)+2H2O(g) ΔH=+534.4 kJ·mol1
D.![]() N2H4(g)+
N2H4(g)+![]() O2(g)
O2(g)![]()
![]() N2(g)+H2O(g) ΔH=16.7 kJ·mol1
N2(g)+H2O(g) ΔH=16.7 kJ·mol1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL 0.01molL﹣1 HA溶液中逐滴加入0.02 molL﹣1 MOH溶液,图中所示的曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中,不正确的是( ) 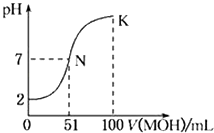
A.HA为一元强酸
B.MOH为一元弱碱
C.N点水的电离程度小于K点水的电离程度
D.K点对应的pH=10,则有c(MOH)+c(OH﹣)﹣c(H+)=0.005molL﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com