
【题目】某固体A在一定条件下加热分解,产物都是气体。分解的方程式为:2A=B↑+2C↑+2D↑。测得生成的混合气体对H2的相对密度为d,则A的相对分子质量为__________。
【答案】5d
【解析】
利用反应的物质的量之比等于化学计量数之比,先设A的物质的量为2mol,则完全反应后生成B、C、D混合气体的总物质的量为5mol,同温同压下密度之比等于摩尔质量之比,求出混合气体的摩尔质量,根据反应前后质量守恒,计算出A的质量,M=m/n,计算出A的摩尔质量,摩尔质量以g/mol为单位时等于相对分子质量。
由2A![]() B↑+2C↑+2D↑可知,设A的物质的量为2mol,则分解生成混合气体的总物质的量为5mol气体,分解产生的混合气体对氢气的相对密度为d,同温同压下,气体的密度之比等于摩尔质量之比,故
B↑+2C↑+2D↑可知,设A的物质的量为2mol,则分解生成混合气体的总物质的量为5mol气体,分解产生的混合气体对氢气的相对密度为d,同温同压下,气体的密度之比等于摩尔质量之比,故![]() (混):
(混):![]() (H2)=M(混):M(H2)= M(混):2g
(H2)=M(混):M(H2)= M(混):2g![]() mol-1,M(混)=
mol-1,M(混)=
2dg![]() mol-1,其质量为2d g
mol-1,其质量为2d g![]() mol-1×5mol=10dg,由质量守恒可知,2molA的质量为10dg,故M(A)=
mol-1×5mol=10dg,由质量守恒可知,2molA的质量为10dg,故M(A)= ![]() =5 d g
=5 d g![]() mol-1,所以A的相对分子质量为5d。
mol-1,所以A的相对分子质量为5d。


科目:高中化学 来源: 题型:
【题目】
有机物A是聚合反应生产胶黏剂基料的单体,亦可作为合成调香剂I、聚酯材料J的原料,相关合成路线如下:

已知:在质谱图中烃A的最大质荷比为118,E的结构简式为:
根据以上信息回答下列问题:
(1) A的分子式为___________,A所含的官能团名称为____________,E→F的反应类型为___________。
(2) I的结构简式为__________________________,
(3) D与新制氢氧化铜悬浊液反应的化学方程式为________________________________。
(4) H的同分异构体W能与浓溴水反应产生白色沉淀,1 mol W参与反应最多消耗3 mol Br2,请写出所有符合条件的W的结构简式_____________________________________。
(5) J是一种高分子化合物,则由C生成J的化学方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物H是一种广谱高效食品防腐剂,如图所示是H分子的球棍模型,下列有关说法正确的是
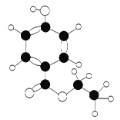
A. 有机物H的分子式为C9H11O3
B. 有机物H的官能团有羟基、羰基和醚键
C. 有机物H能发生加成反应、取代反应和氧化反应
D. 1mol有机物H最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通立德粉(BaSO4·ZnS)广泛用于工业生产中,可利用ZnSO4和BaS共沉淀法制备。以粗氧化锌(含Zn、CuO、FeO等杂质)和BaSO4为原料制备立德粉的流程如下:
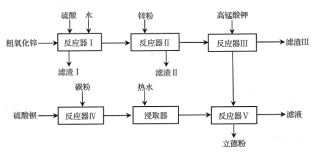
(1)生产ZnSO4的过程中,反应器Ⅰ要保持强制通风,原因是___。
(2)加入锌粉的主要目的是___(用离子方程式表示)。
(3)已知KMnO4在酸性溶液中被还原为Mn2+,在弱酸性、弱碱性溶液中被还原为MnO2,在碱性溶液中被还原为MnO42-。据流程判断,加入KMnO4时溶液的pH应调至___;
a.2.2~2.4 b.5.2~5.4 c.12.2~12.4
滤渣Ⅲ的成分为____。
(4)制备BaS时,按物质的量之比计算,BaSO4和碳粉的投料比要大于1:2,目的是__;生产过程中会有少量氧气进入反应器Ⅳ,反应器Ⅳ中产生的尾气需用碱液吸收,原因是__。
(5)普通立德粉(BaSO4·ZnS)中ZnS含量为29.4%,高品质银印级立德粉中ZnS含量为62.5%。在ZnSO4、BaS、Na2SO4、Na2S中选取三种试剂制备银印级立德粉,所选试剂为___,反应的化学方程式为__(已知BaSO4相对分子质量为233,ZnS相对分子质量为97)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为_______,其沸点比NH3的_______(填“高”或“低”),其判断理由是_________________________。
(2)Fe成为阳离子时首先失去______轨道电子,Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为______________________。
(3)比较离子半径:F__________O2(填“大于”等于”或“小于”)。
(4)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。

图中F和O2共同占据晶胞的上下底面位置,若两者的比例依次用x和1x代表,则该化合物的化学式表示为____________,通过测定密度ρ和晶胞参数,可以计算该物质的x值,完成它们关系表达式:ρ=________g·cm3。
以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为(![]() ),则原子2和3的坐标分别为__________、__________。
),则原子2和3的坐标分别为__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应CCl4+4Na![]() C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
C(金刚石)+4NaCl可实现人工合成金刚石。下列关于该反应的说法错误的是( )
A. C(金刚石)属于原子晶体
B. 该反应利用了Na的强还原性
C. CCl4和C(金刚石)中C的杂化方式相同
D. NaCl晶体中每个Cl-周围有8个Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地球上的海水中蕴藏了大约40万亿吨氘。从1升海水里提取的氘,在聚变反应中所释放的能量,相当于燃烧300升汽油。如果把自然界的氘和氚全部用于聚变反应,释放出来的能量足够人类使用100亿年。与核裂变相比,氘和氚的聚变能是一种安全、不产生放射性物质、原料成本低廉的能源。同温同压下有等质量的H2、D2、T2三种气体,下列叙述正确的是
①密度之比为1∶2∶3 ②质子数之比为6∶3∶2 ③中子数之比为0∶6∶8 ④体积之比为6∶3∶2
A.①②③④B.只有①②C.只有③④D.只有②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙烯醇生产过程中会产生大量副产物乙酸甲酯,其催化醇解反应可用于制备甲醇和乙酸己酯,该反应的化学方程式为:CH3COOCH3(l)+C6H13OH(l)![]() CH3COOC6H13(l)+ CH3OH(l)
CH3COOC6H13(l)+ CH3OH(l)
已知v正=k正·x(CH3COOCH3)·x(C6H13OH),v逆=k逆·x(CH3COOC6H13)·x(C6H13OH),其中v正,v逆为正、逆反应速率,k正,k逆为速率常数,x为各组分的物质的量分数。
(1)反应开始时,己醇和乙酸甲酯按物质的量之比1:1投料,测得348K、343K、338K三个温度下乙酸甲酯转化率(a)随时间(t)的变化关系如图所示。

该醇解反应的ΔH__0(填![]() 或
或![]() )。348K时,以物质的量分数表示的化学平衡常数Kx=__(保留2位有效数字)。
)。348K时,以物质的量分数表示的化学平衡常数Kx=__(保留2位有效数字)。
在曲线①、②、③中,k正-k逆经值最大的曲线是__;A、B、C、D四点中,v正最大的是__,v逆最大的是__。
(2)343K时,己醇和乙酸甲酯按物质的量之比1:1、1:2和2:1进行初始投料.则达到平衡后,初始投料比__时,乙酸甲酯转化率最大;与按1:2投料相比,按2:1投料时化学平衡常数Kx__(填增大、小不变)。
(3)该醇解反应使用离子交换树脂作催化剂,下列关于该催化剂的说法正确的是__。
a.参与了醇解反应,但并不改变反应历程 b.使k正和k逆增大相同的倍数
c.降低了醇解反应的活化能 d.提高乙酸甲酯的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸具有抗氧化、延缓衰老、减肥降脂等功效,它的结构简式为
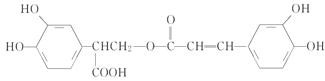 ,以邻苯二酚为原料合成迷迭香酸的路线为
,以邻苯二酚为原料合成迷迭香酸的路线为
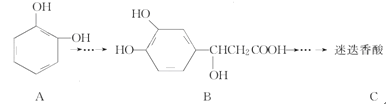
下列说法正确的是
A.有机物B可以发生取代、加成、消去、氧化反应
B.有机物A分子中所有原子一定在同一平面上
C.有机物C在浓硫酸催化下水解的一种产物是B
D.1 mol B与足量的NaOH溶液反应,最多可消耗4 mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com