
(10分)已知:H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式: 、 。
(3)写出Y到Z变化过程的离子方程式: 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: 。
(10分)每空2分。
(1)Cu+H2O2+H2SO4=CuSO4+2H2O
(2)4Fe2++O2+4H+=4Fe3++2H2O 2Fe3++2I—=2Fe2++I2
(3)Fe3++3OH—=Fe(OH)3↓
(4)10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O
解析试题分析:(1)根据图中所示M为红色金属,MSO4为蓝色溶液,可以推知M为Cu。结合题中“H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。”,可知:M溶于稀H2SO4和H2O2混合液的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O。(2)由图中的E+MSO4="M+X," 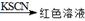 ,可推知E为Fe,X为FeSO4,Fe2+具有还原性,易被氧化成Fe3+,Fe3+具有氧化性,能氧化I—等。因此方程式为:4Fe2++O2+4H+=4Fe3++2H2O 2Fe3++2I—=2Fe2++I2。(3)由上题可知Y中含有Fe3+,Fe3+与OH—生成沉淀,方程式为:Fe3++3OH—=Fe(OH)3↓。(4)由上题可知Z为Fe(OH)3,结合图中所示,方程式为:10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O。
,可推知E为Fe,X为FeSO4,Fe2+具有还原性,易被氧化成Fe3+,Fe3+具有氧化性,能氧化I—等。因此方程式为:4Fe2++O2+4H+=4Fe3++2H2O 2Fe3++2I—=2Fe2++I2。(3)由上题可知Y中含有Fe3+,Fe3+与OH—生成沉淀,方程式为:Fe3++3OH—=Fe(OH)3↓。(4)由上题可知Z为Fe(OH)3,结合图中所示,方程式为:10KOH+3Cl2+2Fe(OH)3=2K2FeO4+6KCl+8H2O。
考点:无机推断
点评:本题考查的是无机的推断,做推断题首先要找到突破口,如本题中突破口是“M为红色金属,MSO4为蓝色溶液”, 可以推知M为Cu。再结合题中所给出的信息一步一步往下分析、解答。推断题考查的内容较广,需要学生对无机物之间的反应熟练在心,才能迎刃而解。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省丹东市高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)已知:H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式: 、 。
(3)写出Y到Z变化过程的离子方程式: 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)已知:![]() H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)
H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:(M、E等字母用所对应的元素符号表示)

(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式: ▲ 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。分别写出上述变黄过程和变蓝过程所发生相关反应的离子方程式: ▲ 、 ▲ 。
(3)写出Y到Z变化过程的离子方程式: ▲ 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式: ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)已知:![]() H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:
H2O2具有较强的氧化性,一些较不活泼金属在稀硫酸存在的情况下,能和H2O2发生氧化还原反应。根据下列框图回答问题:
| |

(1)试推断金属M、E分别是(填元素符号): ▲ 、 ▲ 。Z的化学式: ▲ 。
(2)某同学取X的溶液,加入少量稀硫酸酸化后露置于空气中一段时间,颜色变黄,再加入KI、淀粉溶液,又变为蓝色。试判断X、Y中的金属阳离子分别是: ▲ 、 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com