
 。下列说法不正确的是
。下列说法不正确的是| A.白磷着火点低,在空气中可自燃 |
| B.白磷、红磷互为同素异形体 |
| C.31 g白磷中,含P—P键1.5 mol |
| D.已知P4(白磷,s)+3O2(g)===2P2O3(s) ΔH=-Q kJ·mol-1,则白磷的燃烧热为Q kJ·mol-1 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
| 催化剂 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.在0.10 mol·L-1 NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)+c(CO ) ) |
| B.甲烷的标准燃烧热是890.3 kJ·mol-1,则甲烷燃烧的热化学方程式是: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1 |
| C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 电解 2Cu+O2↑+4H+ |
| D.以KOH为电解质溶液的甲醇燃料电池的负极电极反应式: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B.pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
| C.饱和氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO) |
| D.0.1mol/L的(NH4)2SO4溶液中:c(NH4+) > c(SO42-) > c(H+) > c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
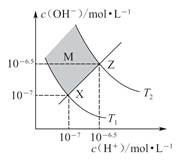
| A.两条曲线间任意点均有c(H+)·c(OH-)=Kw |
| B.M区域内任意点均有c(H+)<c(OH-) |
| C.图中T1<T2 |
| D.XZ线上任意点均有pH=7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
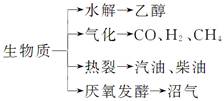
| A.①②③④⑤ | B.①②④⑤ |
| C.③④⑤ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 O2(g)=H2O(l)ΔH=-285.8 kJ/mol
O2(g)=H2O(l)ΔH=-285.8 kJ/mol O2(g)=H2O(g) ΔH=-241.8 kJ/mol
O2(g)=H2O(g) ΔH=-241.8 kJ/mol O2(g)=CO(g)ΔH=-110.5 kJ/mol
O2(g)=CO(g)ΔH=-110.5 kJ/mol查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com