
【题目】下列有关物质性质和应用都正确的是
A.氢氟酸具有强酸性,可用于雕刻玻璃
B.氨气显碱性,可用P2O5或无水CaCl2干燥
C.MgO、Al2O3熔点高,它们都可用于制作耐火材料
D.铜的活动性比铁弱,可在海轮外壳装铜块减缓海轮腐蚀
科目:高中化学 来源: 题型:
【题目】实验室保存下列物质的方法中,不正确的是
A. 少量金属钠保存在煤油里
B. 烧碱溶液盛装在带玻璃塞的磨口玻璃瓶中
C. 新制氯水通常保存在棕色试剂瓶中
D. FeSO4溶液存放在加有少量铁粉的试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于晶体的下列说法正确的是( )
A. 六方最密堆积的空间利用率是52%
B. 离子晶体中一定含金属阳离子
C. 在共价化合物分子中各原子都形成8电子结构
D. 分子晶体的熔点不一定比金属晶体的熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列陈述正确并且有因果关系的是( )
A. SiO2有导电性,可用于制备光导纤维
B. 浓硫酸具有氧化性,可用于干燥H2
C. Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚
D. FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是一种重要的化工原料,工业上生产硝酸的主要过程中:(1)反应N2(g)+3H2(g)![]() 2NH3(g)△H<0 ;恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡下列图像能正确表示该过程中相关量的变化的是__________。(选填字母)。
2NH3(g)△H<0 ;恒温时,将N2和H2的混合气体充入2L密闭容器中,10分钟后反应达到平衡下列图像能正确表示该过程中相关量的变化的是__________。(选填字母)。

(2)一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原来的7/10,则N2的转化率a1=________;
若向该容器中再加入1molN2和3molH2,达到平衡状态时,N2的转化率为a2,则a2________a1(填“>”、“<”或“=”)。
(3)2NO(g)+O2(g)![]() 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。

①比较P1、P2的大小关系:P1____P2(填“>”、“<”或“=”)。
②随温度升高,该反应平衡常数变化的趋势是__________。
(4)硝酸厂常用如下2种方法处理尾气。
①催化还原法:催化剂存在时用H2将NO2还原为N2。
已知:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
则H2还原NO2生成水蒸气反应的热化学方程式是________________________________。
②碱液吸收法:用Na2CO3溶液吸收NO2生成CO2。若每4.6gNO2和Na2CO3溶液反应时转移电子数为0.05mol,则反应的离子方程式是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与氨反应,研究氨的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
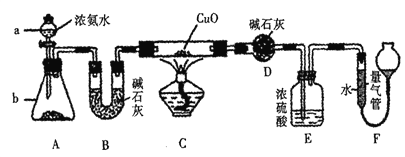
(1)仪器a的名称为 _________。
(2)实验室中,利用装置A,还可制取的无色气体是_________(填字母)。
A.Cl2 B.04 C.C02 D.N02
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管内有无色无味的气体生成,上述现象证明氨气具有________性,写出相应的化学方程式 __________。
(4) D装置的作用是 __________。
(5) E装置中浓硫酸的作用是__________。
(6)读取气体体积前,应对装置F进行的操作是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)请认真观察下图,然后回答问题。
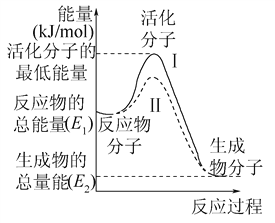
图中所示反应是__________(填“吸热”或“放热”)反应,该反应的ΔH=__________(用含E1、E2的代数式表示)。
(二)已知下列热化学方程式:
①H2(g)+![]() O2(g)===H2O(l) ΔH=-285.8 kJ/mol
O2(g)===H2O(l) ΔH=-285.8 kJ/mol
②H2(g)+![]() O2(g)===H2O(g) ΔH=-241.8 kJ/mol
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③C(s)+![]() O2(g)===CO(g) ΔH=-110.5 kJ/mol
O2(g)===CO(g) ΔH=-110.5 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
回答下列各问题:
(1)H2的燃烧热为__________;C的燃烧热为________。
(2)上述反应中属于放热反应的是__________________。(填序号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com