
��ӦA2+B2 2AB ��H=QkJ/mol���ڲ�ͬ�¶Ⱥ�ѹǿ�ı�������£�����AB�����������ͼ��ʾ��aΪ500�桢bΪ300��������cΪ��Ӧ��300��ʱ��ʱ��t3��ʼ�������м�ѹ�������������������ȷ����
2AB ��H=QkJ/mol���ڲ�ͬ�¶Ⱥ�ѹǿ�ı�������£�����AB�����������ͼ��ʾ��aΪ500�桢bΪ300��������cΪ��Ӧ��300��ʱ��ʱ��t3��ʼ�������м�ѹ�������������������ȷ����

A��A2��B2��AB��Ϊ���壬Q��0
B��ABΪ���壬A2��B2����һ��Ϊ�����壬Q��0
C��ABΪ���壬A2��B2����һ��Ϊ�����壬Q��0
D��ABΪ���壬A2��B2����һ��Ϊ�����壬Q��0

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������ѧ�����нβ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪ijǿ���Ե���Һ�д��ڴ����� �������йظ���Һ�л����ڵ�����������ȷ����
�������йظ���Һ�л����ڵ�����������ȷ����
A����Ԫ������Al3����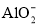 ����ʽ����
����ʽ����
B����Ԫ������Fe2����Fe3������ʽ����
C����Ԫ����Ҫ��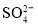 ����ʽ����
����ʽ����
D����Ԫ������Cl����ClO������ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڼ�����Һ���ܴ�����������ҺΪ��ɫ�� ��������
��������
A��K+��Na+��NO3����CO32��
B��K+ ��MnO4����Na+��Cl��
C ��Na+��H+��NO3����SO42��
��Na+��H+��NO3����SO42��
D��Fe3+��Na+��Cl����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�γ��и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��� �Ƶķ����ܴﵽʵ��Ŀ�ĵ���
�Ƶķ����ܴﵽʵ��Ŀ�ĵ���
A���Ʊ�Fe(OH)3���壺��0.1mol��L��1FeCl3��Һ�м�������0.3mol��L��1NaOH��Һ
B����ȥFeCl3��Һ������Cu2+����������Cu2+��FeCl3��Һ�м����������ۣ���ַ�Ӧ�����
C���Ƚ�Fe(OH)3��Al(OH)3���ܶȻ�����0.1mol��L��1FeCl3��Һ�еμ�0.1 mol��L��1
��ˮ�����ٲ���������Ȼ���ٵ���0.1mol��L��1AlCl3��Һ���۲�����
D����֤������Fe3+��Br2��Cl2�����Թ������μ���1mL 0.1mol��L��1Fe Br2��Һ������KSCN��Һ��1mL����Ȼ����μ�����ˮ����������ֱ����ˮ�������۲������������л����ˮ���е�����
Br2��Һ������KSCN��Һ��1mL����Ȼ����μ�����ˮ����������ֱ����ˮ�������۲������������л����ˮ���е�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʱ������4����ҺpH��С����
A��0.02mol/L������Һ��������ˮ���
B��0.02mol/L������0.02mol/LNaOH��Һ��������Һ
C��0.03mol/L������0.01mol/LNaOH��Һ��������Һ
D��pH = 2��������pH = 12��NaOH��Һ��������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�߶�������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��C��s��+CO2��g�� 2CO��g�� ��H��0���÷�Ӧ�ﵽƽ����������������ڷ�Ӧ����������е���
2CO��g�� ��H��0���÷�Ӧ�ﵽƽ����������������ڷ�Ӧ����������е���
A�������¶Ⱥͼ�Сѹǿ B�������¶Ⱥͼ�Сѹǿ
C�������¶Ⱥ�����ѹǿ D�������¶Ⱥ�����ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ����������������������ȷ����
A����״���£�22.4LH2O���еķ�����Ϊ1 NA
B�����³�ѹ��,1.06g Na2CO3���е�Na+������Ϊ0.02 NA
C��ͨ��״���£�1 NA ��CO2����ռ�е����Ϊ22.4L
D�����ʵ���Ũ��Ϊ0.5mol��/L��MgCl2��Һ�У�����Cl- ����Ϊ1 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�����и�����ѧ�����м�⻯ѧ�Ծ��������棩 ���ͣ������
�����������ʡ����ص����ʵ���Ҫԭ�ϡ�
��1���ϳɰ���ӦN2(g) + 3H2(g) 2NH3(g)��һ�����������Է����е�ԭ���� ���绯ѧ���Ǻϳɰ���һ���·�������ԭ����ͼ1��ʾ�������ĵ缫��Ӧʽ�� ��
2NH3(g)��һ�����������Է����е�ԭ���� ���绯ѧ���Ǻϳɰ���һ���·�������ԭ����ͼ1��ʾ�������ĵ缫��Ӧʽ�� ��
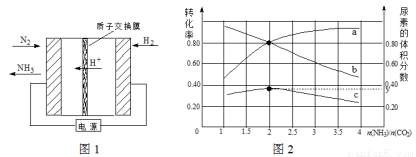
��2����̼��[n(NH3)/n(CO2)]�Ժϳ�����[2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)]��Ӱ�죬���º���ʱ���������ʵ���3 mol��NH3��CO2�Բ�ͬ�İ�̼�Ƚ��з�Ӧ�������ͼ2��ʾ��a��b�߷ֱ��ʾCO2��NH3��ת���ʱ仯��c�߱�ʾƽ����ϵ�����ص���������仯��[n(NH3)/ n(CO2)]= ʱ�����ز���������㣬ͼ��y= ����ȷ��0.01����
CO(NH2)2(g)+H2O(g)]��Ӱ�죬���º���ʱ���������ʵ���3 mol��NH3��CO2�Բ�ͬ�İ�̼�Ƚ��з�Ӧ�������ͼ2��ʾ��a��b�߷ֱ��ʾCO2��NH3��ת���ʱ仯��c�߱�ʾƽ����ϵ�����ص���������仯��[n(NH3)/ n(CO2)]= ʱ�����ز���������㣬ͼ��y= ����ȷ��0.01����
��3����ˮ�к���������Ĵ��������ж��֡�
��NaClO��Һ�ɽ���ˮ�е�NH4+ת��ΪN2�������������в���N2 0.672 L����״����������Ҫ����0.3 mol��L-1��NaClO��Һ L��
��������������£�NH4+����������Ӧ��ת��ΪNO3-��������Ӧ�������仯��ͼ3��ʾ����1 mol NH4+ (aq)ȫ����������NO3- (aq)ʱ�ų��������� kJ��

����H2����ԭ���ɽ���ˮ��NO3-��Ũ�ȣ��õ��IJ����ܲ������ѭ������Ӧ����Һ��pH ������ߡ��������͡����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ��ɰ�һ�С�������и߶�������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£���1 mol N2��3 mol H2��������ܱ������У��ﵽƽ��ʱ�����NH3Ϊ0.8 mol�������ʱ�ټ���1 mol N2��3 mol H2���ﵽ��ƽ��ʱ��NH3�����ʵ���
A������0.8 mol B������1.6 mol
C������0.8 mol��1.6 mol D������1.6 mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com