
| AЁЂ0.05 mol/L |
| BЁЂ0.20 mol/L |
| CЁЂ0.30 mol/L |
| DЁЂ0.40 mol/L |



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂАБЦј | BЁЂСђЫс |
| CЁЂбѕЛЏФЦ | DЁЂСђЫсФЦ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК

| AЁЂХЈHNO3ОпгаЧПбѕЛЏадЃЌФмНЋCЁЂSiЁЂPЗжБ№бѕЛЏГЩCO2ЁЂSiO2ЁЂH3PO4 |
| BЁЂCl2ЁЂSO2ЖМПЩгУгкЦЏАзЃЌАД1ЃК1ЛьКЯЭЈШыЦЗКьШмвКЦЏАзаЇЙћИќМб |
| CЁЂХЈH2SO4гыCuЗДгІжЛБэЯжЦфЧПбѕЛЏад |
| DЁЂNH3МЋвзШмгкЫЎЃЌЕЋПЩгУШчЭМЮќЪеАБ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| дЊЫиДњКХ | L | M | Q | R | T |
| дзгАыОЖ/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| жївЊЛЏКЯМл | +2 | +3 | +2 | +6ЁЂ+4ЁЂ-2 | -2 |
| AЁЂгыЯЁбЮЫсЗДгІЕФОчСвГЬЖШЃКLЕЅжЪЃМQЕЅжЪ |
| BЁЂШШЮШЖЈадЃКH2TЃМH2R |
| CЁЂMгыTаЮГЩЕФЛЏКЯЮяОпгаСНад |
| DЁЂL2+гыR2-ЕФКЫЭтЕчзгЪ§ЯрЕШ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂ9min |
| BЁЂ27min |
| CЁЂ13.5min |
| DЁЂ3min |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
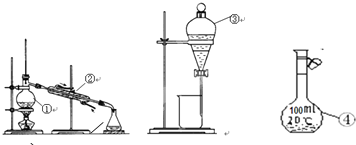
AЁЂ ИЏЪДЦЗ |
BЁЂ БЌеЈЦЗ |
CЁЂ гіЪЊвзШМЦЗ |
DЁЂ бѕЛЏМС |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂКЌзюИпМлдЊЫиЕФЛЏКЯЮяЃЌвЛЖЈОпгаЧПбѕЛЏад |
| BЁЂбєРызгжЛгабѕЛЏадЃЌвѕРызгжЛгаЛЙдад |
| CЁЂЪЇЕчзгдНЖрЃЌЛЙдаддНЧП |
| DЁЂЪєгкбѕЛЏЛЙдЗДгІЕФЛЏКЯЗДгІВЛвЛЖЈЪЧвђЮЊгаЕЅжЪВЮгыСЫЗДгІ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
| AЁЂИФБфЭтНчЬѕМўВЛФмИФБфЛЏбЇЦНКтзДЬЌ |
| BЁЂЕБФГЗДгІдквЛЖЈЬѕМўЯТЗДгІЮязЊЛЏТЪБЃГжВЛБфЪБМДДяЕНСЫЛЏбЇЦНКтзДЬЌ |
| CЁЂЕБФГЗДгІЬхЯЕжаЦјЬхЕФбЙЧПВЛдйИФБфЪБЃЌИУЗДгІвЛЖЈДяЕНЦНКтзДЬЌ |
| DЁЂЕБФГЗДгІДяЕНЦНКтзДЬЌЪБЃЌЗДгІЮяКЭЩњГЩЮяЕФХЈЖШвЛЖЈЯрЕШ |
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com