
 组成元素相同,含有的电子数也相同
组成元素相同,含有的电子数也相同 



 的名称为:1,3-二甲基-2-丁烯
的名称为:1,3-二甲基-2-丁烯| A、①②④⑥ | B、①④⑤⑧ |
| C、①②⑤⑧ | D、②③⑤⑦ |
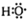 分别为羟基的结构简式和电子式;
分别为羟基的结构简式和电子式;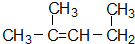 最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;
最长碳链为5个碳原子,从右端开始编号,2号碳上有1个甲基和双键,据此命名;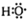 分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;
分别为羟基的结构简式和电子式,组成元素相同,含有的电子数也相同,故①正确;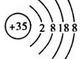 ,故③错误;
,故③错误; ,故④错误;
,故④错误;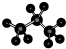 ,故⑤正确;
,故⑤正确; ,故⑥错误;
,故⑥错误;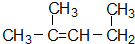 的正确名称为:2-甲基-2-戊烯,故⑦错误;
的正确名称为:2-甲基-2-戊烯,故⑦错误;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
| A | SO2 | sp | 直线形 | 直线形 |
| B | HCHO | sp2 | 平面三角形 | 三角锥形 |
| C | NF3 | sp2 | 四面体形 | 平面三角形 |
| D | NH4+ | sp3 | 正四面体形 | 正四面体形 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 |
| B、若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
| C、X、Y、Z、W的原子半径依次减小 |
| D、W与X形成的化合物中只含离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光线照射时,从侧面可观察到一条光亮的通路 |
| B、加入稀硫酸立即产生沉淀 |
| C、分散质粒子小于1nm |
| D、装入半透膜袋中并将其浸入盛水的烧杯中一段时间,袋内外均含分散质粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al(OH)3和Al3+ |
| B、Al(OH)3和AlO2- |
| C、全部为Al(OH)3 |
| D、全部为AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐类物质一定含有金属离子 |
| B、NaCl固体属于电解质 |
| C、氢氧化铁胶体、硫酸铜溶液都属于介稳体系 |
| D、凡能电离出H+的化合物均为酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com