
【题目】海水占地球总储水量的97.2%.若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是_____(填物理变化、化学变化);
(2)从海水中可获得大量的氯化钠,精制盐水时要除去SO42﹣、Mg2+、Ca2+,可依次加入稍过量的溶液是NaOH、_____、_____(写化学式),过滤后,再加入盐酸,蒸发溶液后可得到较纯净的氯化钠。
(3)食盐水能导电,是因为NaCl能电离出Na+和Cl﹣,它们的电子式分别为_____和_____,工业上利用电解饱和食盐水可制得重要化工产品,该反应的化学方程式_____
(4)氢气用途广泛,完全燃烧4g氢气就能烧开一壶水,在标准状况下,这些氢气的体积是_____L,含_____个氢原子。
(5)将制得的氯气通入石灰乳中可以制得漂粉精,其中有效成份为_____(写名称),漂粉精可用于游泳池中水的消毒,原因是(用化学方程式表示):_____。
【答案】物理变化 BaCl2 Na2CO3 Na+ ![]() 2NaCl+2H2O
2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 44.8 2.408×1024 次氯酸钙 Ca(ClO)2+2CO2+H2O=Ca(HCO3)2+2HClO
2NaOH+H2↑+Cl2↑ 44.8 2.408×1024 次氯酸钙 Ca(ClO)2+2CO2+H2O=Ca(HCO3)2+2HClO
【解析】
(1)根据蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水分析判断;
(2)根据SO42-、Ca 2+、Mg2+等易转化为沉淀而被除去,前面加入的过量溶液应用后面加入的溶液除去,据此分析选择除杂试剂和顺序;
(3)钠离子是阳离子,氯离子是阴离子,根据电子式的书写方法书写;电解饱和食盐水生成氢氧化钠、氢气和氯气,据此书写反应的方程式;
(4)根据n=![]() =
=![]() =
=![]() 计算;
计算;
(5)氯气能够与氢氧化钙反应生成氯化钙、次氯酸钙和水,漂粉精成分为氯化钙和次氯酸钙的化合物,其中次氯酸钙能够与空气中的二氧化碳和水反应生成次氯酸,次氯酸具有强氧化性,能够杀菌消毒,据此分析解答。
(1)蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,水的状态变化,属于物理变化,故答案为:物理变化;
(2)SO42﹣、Mg2+、Ca2+等分别与BaCl2溶液、NaOH溶液、Na2CO3溶液反应生成沉淀,再过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,盐酸能除去过量的Na2CO3溶液和NaOH溶液,所以应先加BaCl2溶液再加NaOH或先加NaOH溶液再加BaCl2溶液、Na2CO3溶液,过滤后,加入盐酸,蒸发溶液后可得到较纯净的氯化钠,故答案为:BaCl2;Na2CO3;
(3)钠离子是阳离子,原子失去最外层电子形成,钠离子的电子式Na+,氯离子是氯原子得到一个电子形成的,需要表示出最外层电子和所带电荷数,氯离子的电子式为:![]() ,电解饱和食盐水生成氢氧化钠、氢气和氯气,反应的化学方程式为:2NaCl+2H2O
,电解饱和食盐水生成氢氧化钠、氢气和氯气,反应的化学方程式为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,故答案为:Na+;
2NaOH+H2↑+Cl2↑,故答案为:Na+;![]() ;2NaCl+2H2O
;2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(4)4g氢气的物质的量=![]() =2mol,在标准状况下,这些氢气的体积=22.4L/mol×2mol=44.8L,含有氢原子个数=2mol×6.02×1023/mol×2=2.408×1024,故答案为:44.8;2.408×1024;
=2mol,在标准状况下,这些氢气的体积=22.4L/mol×2mol=44.8L,含有氢原子个数=2mol×6.02×1023/mol×2=2.408×1024,故答案为:44.8;2.408×1024;
(5)氯气能够与氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,其中漂粉精的有效成份为次氯酸钙[Ca(ClO)2],次氯酸钙能够与空气中的二氧化碳和水反应生成次氯酸,Ca(ClO)2+2CO2+H2O=Ca(HCO3)2+2HClO,次氯酸具有强氧化性,能够杀菌消毒,故答案为:次氯酸钙;Ca(ClO)2+2CO2+H2O=Ca(HCO3)2+2HClO。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
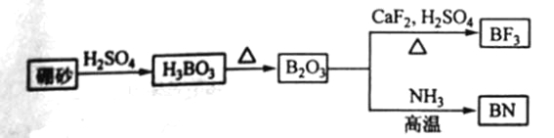
请回答下列问题:
(1) 由B2O3制备BF3、BN的化学方程式依次是_________、__________;
(2) 基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(3) 在BF3分子中,F-B-F的建角是_______,B原子的杂化轨道类型为_______,BF3和过量NaF作用可生成NaBF,BF的立体结构为_______;
(4) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶苞边长为361.5pm,立方氮化硼晶苞中含有______各氮原子、________各硼原子,立方氮化硼的密度是_______g·![]() (只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同分异构现象在有机物中广泛存在,如图为苯及其几种同分异构体的键线式,下列有关说法中正确的是

A. b、c均与乙烯互为同系物
B. a和d的二氯代物均有3种
C. 4种有机物均能使酸性高锰酸钾溶液褪色
D. a和b中所有原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学反应原理研究碳、硫及其化合物的性质具有重要意义。
(1)工业上用炭还原辉铜矿(主要成分是Cu2S),可制取金属铜。
已知反应的热化学方程式如下:
C(s)+S2 (g) ═CS2 (g) △H1=150 KJ/mol
Cu2S(s)+H2 (g) ═2Cu(s)+H2S (g) △H2=59.5KJ/mol
2H2S (g) ═2H2 (g) +S2 (g) △H3=170KJ/mol
通过计算,可知用炭还原Cu2S 制取金属铜和CS2(g) 的热化学方程式为___________。
(2)为研究反应2H2S(g)![]() 2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
2H2(g)+S2(g)对上述工业过程的影响,兴趣小组进行如下探究:
①向三个体积均为1L的恒容密闭容器中分别加入1molH2S,进行H2S分解实验。不同温度下测得H2S 的转化率与时间的关系如图1所示:

T1温度下,0~5min S2(g)的平均反应速率v(S2)=____________mol.L-1.min-1,反应平衡常数K=_____molL-1.温度T1、T2、T3 由高到低的顺序是__________。
②T4温度时,向1L的恒容密闭容器中加入1.8molH2(g)、1.2molS2(g),达到平衡后测得S2(g)和H2S(g)的浓度相等,则T4_____ T1 (填“<”、“=”或“>”)。
(3)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH 溶液,所得溶液中三种微粒H2C2O4、HC2O4-、C2O42- 的物质的量分数(δ) 与pH的关系如图2所示:
①草酸的电离常数分别为K1与K2,则![]() =_____。
=_____。
②按投料比n(Na2C2O4):n(NaHC2O4)=2:1配成溶液,下列有关该溶液的叙述正确的是_____(填序号)。
A.该溶液的pH为4.2
B.3c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+2c(C2O42-)
C.3c(Na+)=5[c(HC2O4-)+c(C2O42-)+c(H2C2O4)]
D.3c(OH-)+c(C2O42-)=3c(H+)+2c(HC2O4-)+5c(H2C2O4)
(4)含碳的甲醇(CH3OH)的废水随意排放会造成水污染,可用ClO2将其氧化为CO2,然后再加碱中和即可。
①写出处理甲醇酸性废水过程中,ClO2与甲醇反应的离子方程式:___________________。
②常温下,向100 mL0.1mol/L的NaOH溶液中通入一定量的CO2。为探究反应后混合溶液的成分,向其中逐滴加入0.1 mol/L的HCl溶液。溶液产生气体前,消耗V( HCl)=V1;溶液刚好不再产生气体时,消耗V( HCl) =V2。当V1 <V2 <2Vl时,混合溶液中溶质的成分为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A. H2SO3的电离方程式:H2SO3![]() 2H++SO32-
2H++SO32-
B. NaHSO4在水溶液中的电离方程式: NaHSO4= Na++H++SO42-
C. Na2CO3的水解∶CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. NH4Cl的水解:NH4++H2O = NH3·H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. N2(g)![]() NH3(g)
NH3(g)![]() NH4Cl(aq)
NH4Cl(aq)
B. Fe(s)![]() FeCl2(s)
FeCl2(s)![]() Fe(OH)2(s)
Fe(OH)2(s)
C. MgO(s)![]() MgSO4(aq)
MgSO4(aq)![]() Mg(s)
Mg(s)
D. S(s)![]() SO2(g)
SO2(g)![]() BaSO3(s)
BaSO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL 0.1mol·L-1 NaOH溶液中加入0.1mol·L-1的一元酸HA溶液,pH变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. b点所示溶液中c(A-)>c(HA)
D. pH=7时,c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 配制FeCl3溶液时,向溶液中加入少量盐酸
B. 实验室用排饱和食盐水的方法收集氯气
C. 往醋酸溶液中加少量碱,有利于CH3COO-的增多
D. H2、I2、HI平衡时的混合气体加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于分离或提纯物质的方法有:①过滤 ②蒸馏 ③加热 ④分液(在下列空白中填写分离提纯的合理方法的序号及装置下合理的选项)。

(1)除去石灰水中悬浮的CaCO3颗粒:________。
(2)提纯氯化钠溶液中的氯化钠:___。
(3)分离汽油和煤油的混合物:______。
(4)分离水和苯的混合物:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com