
����Ŀ���Ƽ����������������̿ɽ���ת��Ϊ��п�����壺

��֪���ٻƼ�������������Ҫ��Fe2O3��ʽ���ڣ�п��Ҫ������п(ZnSO4)������п(ZnO)������п(ZnSiO3)��ʽ���ڣ��Ƽ���������ijЩԪ�سɷ����±���ʾ��
Ԫ�� | Fe | Zn | Cu | Cd | Ca | Mg | Si |
�������� | 28.9 | 8.77 | 0.37 | 0.18 | 0.37 | 0.84 | 4.63 |
��NH4F��Һ���ڳ���Mg2+��Ca2+����Fe��Cd�Ľ���������
���������������1����Ҫ�ɷ�Ϊ________(д��ѧʽ)��Ϊ����߽����ʣ��ɲ�ȡ�Ĵ�ʩ��________(д��һ�ּ���)��
������ԭ�����������У�����������Ϊ�˳�ȥ��Һ��________��________�Ƚ����������ӡ�
�Ǽ���(NH4)2S����Cd2+ʱӦ���������ԭ����________�����˹�������Һ����ʱ���������ᵼ��Cd2+ȥ����ƫ�ͣ�ԭ����________��(��֪��CdS���ܶȻ�Ksp = 8��10��27��FeS���ܶȻ�Ksp = 4��10��19��ZnS���ܶȻ�Ksp = 1.6��10��24)
��д����������������������FeCO3�����ӷ�Ӧ����ʽΪ��________��
����п��������һ����Ҫ�Ĵ��Բ��ϡ��ⶨ��������ZnO��ʵ�鲽�����£�

��д������(Mn2+)�����е����ӷ���ʽ________��
��ȷ��ȡ25.00 mL��ҺA���ڱ������ö��ӳ���ָʾ������0.0100mol/L��EDTA(Na2H2Y)����Һ�ζ����е�Zn2+ (��Ӧԭ��ΪZn2+ + H2Y2�� =ZnY 2�� + 2H+)�����ζ��յ�ʱ����EDTA����Һ20.00 mL��ͨ������ȷ������������ZnO����������Ϊ________��
���𰸡�H2SiO3�� �ʵ��������Ũ�ȡ�����¶ȡ����衢����ԭ��![]() ��������
��������![]() Fe3+ Cu2+ (NH4)2S������Fe2+��Zn2+��ת��ΪFeS��ZnS���������Fe2+��Zn2+��ʧ ������ʱ�����ʱ������Fe2+���������Fe3+��Fe3+����S2��������Ӧ��ʹS2��Ũ���½����Ӷ�����ȥ���ʽ���(Ҳ����O2��S2�����������S2��Ũ���½�) 2HCO3�� + Fe2+ = H2O + FeCO3��+ CO2���� S2O82�� + 2H2O +Mn2+ = 2SO42�� + MnO2�� + 4H+ 16.20%
Fe3+ Cu2+ (NH4)2S������Fe2+��Zn2+��ת��ΪFeS��ZnS���������Fe2+��Zn2+��ʧ ������ʱ�����ʱ������Fe2+���������Fe3+��Fe3+����S2��������Ӧ��ʹS2��Ũ���½����Ӷ�����ȥ���ʽ���(Ҳ����O2��S2�����������S2��Ũ���½�) 2HCO3�� + Fe2+ = H2O + FeCO3��+ CO2���� S2O82�� + 2H2O +Mn2+ = 2SO42�� + MnO2�� + 4H+ 16.20%
��������
�����������п(ZnSiO3)�еĹ�����������ӽ�ϳɹ��������Ϊ����߽����ʣ��ɲ�ȡ�Ĵ�ʩ���ʵ��������Ũ�ȡ�����¶ȡ����衢����ԭ�ϵȡ�
�ơ���ԭ���ӡ������У�������������ԭ����ʹ������ת��Ϊ�������ӣ�ʹͭ����ת��Ϊ����ͭ��
����CdS��FeS��ZnS���ܶȻ���֪����(NH4)2S��������������������Fe2+��Zn2+��Ӧ������FeS��ZnS���������˹�������Һ����ʱ�����������Fe2+���������Fe3+��Fe3+����S2��������Ӧ��
�ȹ�����������̼��������������ӷ�Ӧ����FeCO3��ͬʱ�ж�����̼���ɣ�����Ԫ���غ㣬����غ�д�����ӷ�Ӧ����ʽ��
�ɢٳ���(Mn2+)������(NH4)2S2O8�������ӷ���������ԭ��Ӧ��S2O82������ԭΪ������������ӱ�����Ϊ�������̣���ʧ�����غ㣬Ԫ���غ�д����Ӧ�����ӷ���ʽ�����ݹ�ϵʽ���м��㡣
�š����������п(ZnSiO3)�еĹ�����������ӽ�ϳɹ����������������1����Ҫ�ɷ�ΪH2SiO3��Ϊ����߽����ʣ��ɲ�ȡ�Ĵ�ʩ���ʵ��������Ũ�ȡ�����¶ȡ����衢����ԭ�ϵȣ��ʴ�Ϊ��H2SiO3���ʵ��������Ũ�ȡ�����¶ȡ����衢����ԭ�ϡ�
�ơ���ԭ���ӡ������У�������������ԭ����ʹ������ת��Ϊ�������ӣ�ʹͭ����ת��Ϊ����ͭ���ʴ�Ϊ��Fe3+��Cu2+��
����CdS��FeS��ZnS���ܶȻ���֪����(NH4)2S��������������������Fe2+��Zn2+��Ӧ������FeS��ZnS���������Fe2+��Zn2+��ʧ�����˹�������Һ����ʱ�����������Fe2+���������Fe3+��Fe3+����S2��������Ӧ��ʹS2��Ũ���½����Ӷ�����ȥ���ʽ��ͣ�
�ʴ�Ϊ��(NH4)2S������Fe2+��Zn2+��ת��ΪFeS��ZnS���������Fe2+��Zn2+��ʧ��������ʱ�����ʱ������Fe2+���������Fe3+��Fe3+����S2��������Ӧ��ʹS2��Ũ���½����Ӷ�����ȥ���ʽ��ͣ�(Ҳ����O2��S2�����������S2��Ũ���½�)��
�ȹ�����������̼��������������ӷ�Ӧ����FeCO3��ͬʱ�ж�����̼���ɣ�����Ԫ���غ㣬����غ㣬���ӷ�Ӧ����ʽΪ2HCO3�� + Fe2+ = H2O + FeCO3��+ CO2�����ʴ�Ϊ��2HCO3�� +Fe2+ = H2O + FeCO3��+ CO2����
�ɢٳ���(Mn2+)������(NH4)2S2O8�������ӷ���������ԭ��Ӧ��S2O82������ԭΪ������������ӱ�����Ϊ�������̣���ʧ�����غ㣬Ԫ���غ㣬�÷�Ӧ�����ӷ���ʽΪS2O82�� + 2H2O +Mn2+ = 2SO42�� + MnO2�� + 4H+���ʴ�Ϊ��S2O82�� + 2H2O +Mn2+ = 2SO42�� + MnO2�� + 4H+��
�ڵζ��յ�ʱ����EDTA����Һ20.00 mL��EDTA��Ũ��Ϊ0.0100mol/L�����ʵ���Ϊ![]() ����п���ӵ����ʵ���Ҳ��
����п���ӵ����ʵ���Ҳ��![]() ������Ԫ���غ㣬����п�����ʵ���Ҳ��
������Ԫ���غ㣬����п�����ʵ���Ҳ��![]() ������25.00 mL��ҺA�к���ZnO�����ʵ���Ϊ
������25.00 mL��ҺA�к���ZnO�����ʵ���Ϊ![]() ����250mL��ҺA������п�����ʵ���Ϊ
����250mL��ҺA������п�����ʵ���Ϊ![]() ������1.0g��Ʒ������п������Ϊ����Ϊ
������1.0g��Ʒ������п������Ϊ����Ϊ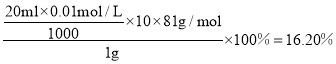 ��
��
�ʴ�Ϊ��16.20%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ͻ����������Ⱦ��Ϊ���ء��ش���������
��1������ѡ���������ص���п��������ձ���Ҫ��Ⱦ�����_____
A��CO2 B.SO2 C������������� D��H2S
��2������β��������CO��NO���ж����壬��������������NO�Ļ�ѧ����ʽ��___________
��3������������װ�е���Ԫ��װ�ã���������CO��NO�ȵ���Ⱦ����Ӧ�������£���Pt����Ϊ����
I��NO��Pt(S)=NO(S)(Pt(S)��ʾ������NO(S)��ʾ����̬NO����ͬ)
II��CO��Pt(S)=CO(S)
III��NO(S)=N(S)��O(S)
IV��CO(S)��O(S)=CO2��2Pt(S)
V��N(S)��N(S)=N2��2Pt(S)
VI��NO(S)��N(S)=N2O��2Pt(S)
β���з�Ӧ�P������Ũ�����¶ȵı仯��ϵ����ͼ��
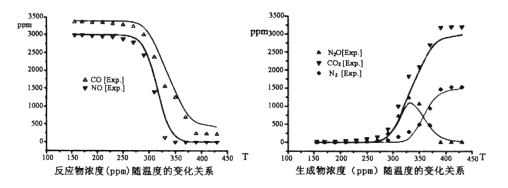
�ش���������
������β�����۷�Ӧ�����˵ķ�Ӧ�¶���____
A. 250�� B.300�� C.330�� D.400��
��330�����µĵ�������������Ҫ��Ӧ�Ļ�ѧ����ʽ��___________
�۵�����N2Oѡ���Ը���N2���ɴ˿��ƶϳ���V��Ӧ�Ļ��____����Ӧ�Ļ�ܣ���
��<������>����=������������_______________
�ܽ�Ϸ�Ӧ������ͼ���¶�λ��330�桪400��ʱ�������¶ȣ�V��Ӧ�ķ�Ӧ����_____�������������С�����䡱����ͬ��������Ӧ�ķ�Ӧ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�ܱ������г�������ʵ���������A��B��һ���¶��·�����ӦA(g)+xB(g) ![]() 2C(g)���ﵽƽ���ֻ�ı䷴Ӧ��һ��������������������ʵ�Ũ�ȡ���Ӧ������ʱ��ı仯����ͼ��ʾ������˵������ȷ��
2C(g)���ﵽƽ���ֻ�ı䷴Ӧ��һ��������������������ʵ�Ũ�ȡ���Ӧ������ʱ��ı仯����ͼ��ʾ������˵������ȷ��
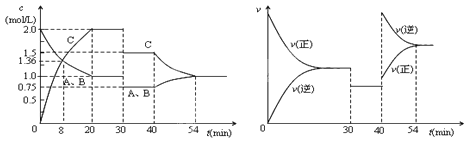
A.ǰ8min A��ƽ����Ӧ����Ϊ0.08mol/(L��s)
B.30minʱ���������������40minʱ�����¶�
C.��Ӧ����ʽ�е�x��1������ӦΪ���ȷ�Ӧ
D.30min��54min�ķ�Ӧ��ƽ�ⳣ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2 L���ܱ������з���4mol N2O5���������·�Ӧ��2N2O5(g)![]() 4NO2(g)+O2(g)����Ӧ���е�5minʱ�����N2O5ת����20%����
4NO2(g)+O2(g)����Ӧ���е�5minʱ�����N2O5ת����20%����
(1)5minʱ��ʣ��N2O5�����ʵ���________��
(2)ǰ5min��v(NO2)Ϊ����__________��
(3)5minʱ��O2�����ʵ���ռ������������ʵ����İٷֱ�_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������߷��ļ��ڣ���������β����ȼúβ�������������ԭ��֮һ��
��1��ʹ�ü״����Ϳ��Լ�������β���Ի�������Ⱦ����ҵ����200���10MPa�������¿��ü��������ͨ��ͭ�ƹܵ���Ӧ�Ƶü״�����֪һ�������£�CH4��CH3OH��ȼ���ȷֱ�784kJ/mol��628kJ/mol ,��CH4(g) +![]() O2(g) = CH3OH(g) ��H=___��
O2(g) = CH3OH(g) ��H=___��
��2��������Ҳ�������Դ���úϳ����ڴ����������Ʊ������ѵķ�Ӧԭ��Ϊ:2CO(g) + 4H2(g) ![]() CH3OCH3(g) + H2O(g) ��H��0��
CH3OCH3(g) + H2O(g) ��H��0��
��.ij�¶��£���2.0molCO(g)��6.0molH2(g)�����ݻ�Ϊ2L���ܱ������У���Ӧ����ƽ��ʱ���ı�ѹǿ���¶ȣ�ƽ����ϵ�� CH3OCH3(g) �����ʵ��������仯�����ͼ��ʾ�������¶Ⱥ�ѹǿ�Ĺ�ϵ�ж���ȷ����___��
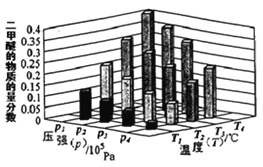
A. P1��P3, T1��T3 ��B. P3��P2��T3��T2 ����C.P2��P4��T4��T2 ����D.P1��P4��T2��T3
���ں����ܱ������ﰴ�����Ϊ1:3����һ����̼���� ����һ�������·�Ӧ�ﵽƽ��״̬�����ı䷴Ӧ��ijһ�����������б仯��˵��ƽ��һ�����淴Ӧ�����ƶ�����___
A��������ת���ʼ�С B���淴Ӧ������������С
C����ѧƽ�ⳣ��Kֵ���� D��ij��Ӧ�������ٷֺ�������
��3����һ�ݻ��ɱ���ܱ������г���10 mol CO��20 mol H2, ������ӦCO(g)��2H2(g) ![]() CH3OH(g)��CO��ƽ��ת����[���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)��CO��ƽ��ת����[���¶�(T)��ѹǿ(p)�Ĺ�ϵ��ͼ��ʾ��

��A��B��C�����Ӧ��ƽ�ⳣ��KA��KB��KC�Ĵ�С��ϵΪ______��
�����ﵽƽ��״̬Aʱ�����������Ϊ10 L������ƽ��״̬Bʱ���������Ϊ________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.50 mol��L��1������50 mL 0.55 mol��L��1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺

(1)��ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ���������________��
(2)�ձ���������ֽ����������________��
(3)���ձ����粻��Ӳֽ�壬��õ��к�����ֵ____________(����ƫ��������ƫС��������Ӱ����)��
(4)��ʵ�鳣��0.50 mol��L��1 HCl��0.55 mol��L��1 NaOH��Һ��50 mL����ʵ�飬����NaOH��ҺŨ�ȴ�������Ũ�ȵ�������______�������µ���10 ��ʱ����ʵ�飬��ʵ��������ɽϴ������ԭ����_____________��
(5)ʵ���и���60 mL 0.50 mol��L��1������50 mL 0.50 mol��L��1 NaOH��Һ���з�Ӧ��������ʵ����ȣ�����õ��к���________(��������������������)���������ɣ� ______________��
(6)����ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к�����H��________(����ƫ��������ƫС��������Ӱ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D����Ԫ�أ����ǵ�ԭ����������������С��18��A��B��ͬһ���ڣ�A�ĵ���ʽΪ��![]() ����Bԭ��L��ĵ���������K���3����0.1 mol C�����ܴ������û���2.24 L(��״��)������ͬʱ���ĵ��Ӳ�ṹ�������ԭ����ͬ�ĵ��Ӳ�ṹ��D���ӵİ뾶��C���ӵ�С��D������B���ӵĵ��Ӳ�ṹ��ͬ��
����Bԭ��L��ĵ���������K���3����0.1 mol C�����ܴ������û���2.24 L(��״��)������ͬʱ���ĵ��Ӳ�ṹ�������ԭ����ͬ�ĵ��Ӳ�ṹ��D���ӵİ뾶��C���ӵ�С��D������B���ӵĵ��Ӳ�ṹ��ͬ��
(1)д��A��B��C��DԪ�ص����ƣ�A________��B______��C________��D________��
(2)DԪ�������ڱ������ڵ�________����______�塣
(3)�õ���ʽ��ʾA����̬�⻯����γɹ��̣�____________��
(4)A��B�ĵ��ʳ�ַ�Ӧ���ɵĻ�����Ľṹʽ��___________��
(5)B��C�γɵĻ����������ӻ����ﻹ�ǹ��ۻ�������֤����_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ѧϰС����ѧϰ��Na2O2��CO2�ķ�Ӧ����ΪNa2O2��SO2Ӧ��Ҳ���Է�Ӧ�������������ͼװ��![]() �г�װ������ȥ��װ�õ�����������
�г�װ������ȥ��װ�õ�����������![]() ����ʵ�飬̽��Na2O2��SO2��Ӧ�IJ���밴Ҫ��ش��������⡣
����ʵ�飬̽��Na2O2��SO2��Ӧ�IJ���밴Ҫ��ش��������⡣
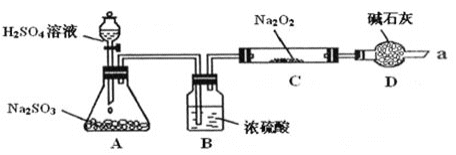
��д��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��_________
��װ��D�����ã����˿��Է�ֹ�����е�CO2��ˮ�����Ƚ���C����Na2O2��Ӧ��������__________��
����ͨ��������SO2��Na2O2��ַ�Ӧ�����Ƕ�C�й������������¼��裺
����1��ֻ��Na2SO3��
����2��_________��
����3������Na2SO3������Na2SO4��
a��Ϊ��һ��ȷ��C�з�Ӧ��������ijɷ�(Na2O2�ѷ�Ӧ��ȫ)����ͬѧ���������ʵ�飺

��ͬѧ�ɴ˵ó����ۣ�������Na2SO4���÷����Ƿ����__________![]() ����������������
����������������![]() ��������_______��
��������_______��
b��������2������д��SO2��Na2O2��Ӧ�Ļ�ѧ����ʽ��_________��
c����ͬѧ���������ʵ���һ��ȷ�ϲ���ijɷ֡�
ʵ�鲽�� | ���� |
��ȡ����C�й���������Թ��У���������������ˮ�ܽ⡣ | ����ȫ���ܽ� |
�������Թ��м��������ϡ���ᣬ�����ɵ�����ͨ����������KMnO4��Һ�С� | ����KMnO4��Һ��ɫ |
������ڷ�Ӧ����Թ��У�����������BaCl2��Һ�� | ������ɫ���� |
������н�����������ͨ����������KMnO4��Һ�У�������Ӧ�����ӷ���ʽΪ�� ________��ͨ������ʵ������ȷ������__________������(ѡ��1��2��3)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ƫ��������N2O4�dz��õĻ���ƽ��������߷������»�ѧ��Ӧ��
(��)(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)
(��)N2O4(g)2NO2(g)
��1����Ӧ(��)����������___��
��2�����¶�����ʱ��������ɫ�����Ӧ(��)Ϊ___(��������������������)��Ӧ��
��3��������ͬ�¶��£�������Ӧ�������Ϊ1L�ĺ����ܱ������н��У�ƽ�ⳣ��___(������������������������С��)����Ӧ3s��NO2�����ʵ���Ϊ0.6mol����0��3s�ڵ�ƽ����Ӧ����v(N2O4)=_______molL-1s-1��
��4��NO2���ð�ˮ��������NH4NO3��25��ʱ����amolNH4NO3����ˮ����Һ�����ԣ�ԭ����___(�����ӷ���ʽ��ʾ)��
��5�������Һ�μ�bL��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫___(��������������������������)�ƶ������μӰ�ˮ��Ũ��Ϊ___mol��L-1��(NH3��H2O�ĵ���ƽ�ⳣ��ȡKb=2��10-5mol��L-1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com