
����Ŀ��ƫ��������N2O4�dz��õĻ���ƽ��������߷������»�ѧ��Ӧ��
(��)(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)
(��)N2O4(g)2NO2(g)
��1����Ӧ(��)����������___��
��2�����¶�����ʱ��������ɫ�����Ӧ(��)Ϊ___(��������������������)��Ӧ��
��3��������ͬ�¶��£�������Ӧ�������Ϊ1L�ĺ����ܱ������н��У�ƽ�ⳣ��___(������������������������С��)����Ӧ3s��NO2�����ʵ���Ϊ0.6mol����0��3s�ڵ�ƽ����Ӧ����v(N2O4)=_______molL-1s-1��
��4��NO2���ð�ˮ��������NH4NO3��25��ʱ����amolNH4NO3����ˮ����Һ�����ԣ�ԭ����___(�����ӷ���ʽ��ʾ)��
��5�������Һ�μ�bL��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫___(��������������������������)�ƶ������μӰ�ˮ��Ũ��Ϊ___mol��L-1��(NH3��H2O�ĵ���ƽ�ⳣ��ȡKb=2��10-5mol��L-1��
���𰸡�N2O4 ���� ���� 0.1 NH4++H2ONH3��H2O+H+ ���� ![]()
��������
��1����������ԭ��Ӧ�л��ϼ۽��͵ķ�Ӧ������������
��2�������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ���
��3����ѧƽ�ⳣ��ֻ���¶��йأ�����![]() ���м��㣻
���м��㣻
��4������笠�����ˮ������ش�
��5������ͬ����ЧӦ��һˮ�ϰ���笠�����ˮ�����������ã�����һˮ�ϰ��ĵ���ƽ�ⳣ������õ���ˮŨ�ȡ�
![]() ��Ӧ
��Ӧ![]() ��
��![]() ��
�У�![]() ��NԪ�صõ��ӻ��ϼ۽��ͣ�
��NԪ�صõ��ӻ��ϼ۽��ͣ�![]() ����������
����������![]() ��CԪ�غ�NԪ�ػ��ϼ����ߣ��ǻ�ԭ�����ʴ�Ϊ��
��CԪ�غ�NԪ�ػ��ϼ����ߣ��ǻ�ԭ�����ʴ�Ϊ��![]() ��
��
![]() �����¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ������¶�����ʱ��������ɫ���ƽ��������Ӧ�����ƶ�����������Ӧ�����ȷ�Ӧ���ʴ�Ϊ�����ȣ�
�����¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ������¶�����ʱ��������ɫ���ƽ��������Ӧ�����ƶ�����������Ӧ�����ȷ�Ӧ���ʴ�Ϊ�����ȣ�
![]() ��ѧƽ�ⳣ��ֻ���¶��йأ������ʵ�Ũ���أ�����ƽ�ⳣ��K���䣻
��ѧƽ�ⳣ��ֻ���¶��йأ������ʵ�Ũ���أ�����ƽ�ⳣ��K���䣻![]() ����
����![]() ���ʴ�Ϊ�����䣻
���ʴ�Ϊ�����䣻![]() ��
��
![]() ���ð�ˮ��������
���ð�ˮ��������![]() ʱ����
ʱ����![]() ����ˮ����Һ�����ԣ�����Ϊ笠�����ˮ�⣻��Ӧ�����ӷ���ʽΪ��
����ˮ����Һ�����ԣ�����Ϊ笠�����ˮ�⣻��Ӧ�����ӷ���ʽΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
![]() ���백ˮ��Һ����笠�����ˮ�⣬ƽ��������У���
���백ˮ��Һ����笠�����ˮ�⣬ƽ��������У���![]() ����ˮ�������Һ�μ�
����ˮ�������Һ�μ�![]() ��ˮ����Һ�����ԣ����ݵ���غ�����֪����Һ������������Ũ��
��ˮ����Һ�����ԣ����ݵ���غ�����֪����Һ������������Ũ��![]() ��
��![]() ��
��![]() �ĵ���ƽ�ⳣ��ȡ
�ĵ���ƽ�ⳣ��ȡ![]() ����Ϻ���Һ���ΪbL��
����Ϻ���Һ���ΪbL��![]() ������һˮ�ϰ�����ƽ��õ���
������һˮ�ϰ�����ƽ��õ���![]() ��ƽ�ⳣ��
��ƽ�ⳣ��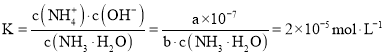 ������õ�
������õ�![]() ���ʴ�Ϊ������
���ʴ�Ϊ������![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ƽ����������������̿ɽ���ת��Ϊ��п�����壺

��֪���ٻƼ�������������Ҫ��Fe2O3��ʽ���ڣ�п��Ҫ������п(ZnSO4)������п(ZnO)������п(ZnSiO3)��ʽ���ڣ��Ƽ���������ijЩԪ�سɷ����±���ʾ��
Ԫ�� | Fe | Zn | Cu | Cd | Ca | Mg | Si |
�������� | 28.9 | 8.77 | 0.37 | 0.18 | 0.37 | 0.84 | 4.63 |
��NH4F��Һ���ڳ���Mg2+��Ca2+����Fe��Cd�Ľ���������
���������������1����Ҫ�ɷ�Ϊ________(д��ѧʽ)��Ϊ����߽����ʣ��ɲ�ȡ�Ĵ�ʩ��________(д��һ�ּ���)��
������ԭ�����������У�����������Ϊ�˳�ȥ��Һ��________��________�Ƚ����������ӡ�
�Ǽ���(NH4)2S����Cd2+ʱӦ���������ԭ����________�����˹�������Һ����ʱ���������ᵼ��Cd2+ȥ����ƫ�ͣ�ԭ����________��(��֪��CdS���ܶȻ�Ksp = 8��10��27��FeS���ܶȻ�Ksp = 4��10��19��ZnS���ܶȻ�Ksp = 1.6��10��24)
��д����������������������FeCO3�����ӷ�Ӧ����ʽΪ��________��
����п��������һ����Ҫ�Ĵ��Բ��ϡ��ⶨ��������ZnO��ʵ�鲽�����£�

��д������(Mn2+)�����е����ӷ���ʽ________��
��ȷ��ȡ25.00 mL��ҺA���ڱ������ö��ӳ���ָʾ������0.0100mol/L��EDTA(Na2H2Y)����Һ�ζ����е�Zn2+ (��Ӧԭ��ΪZn2+ + H2Y2�� =ZnY 2�� + 2H+)�����ζ��յ�ʱ����EDTA����Һ20.00 mL��ͨ������ȷ������������ZnO����������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���õ��з�̪���Ȼ�����Һʪ�����ֽ�ֱ����ס�������ʵ�飬�����жϴ�����ǣ� ��

A.b������������ð��B.d���������ֺ�ɫ
C.a��c���϶�����������ӦD.����������������������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���һ����̼��ԭ��������ʵ�������IJ������Ũ����Ȥ����ͨ��ʵ����̽����ɷ֡�
����ʵ��װ�ã�

��װ��B�з��������ӷ���ʽ�� ______��װ��B�������� ______��
����ʵ����������A�еķ�ĩ�ɺ�ɫ��Ϊ��ɫʱ��ֹͣ���ȣ�����ͨһ����̼����ȴ�����£�ֹͣͨ����ͬʱ�۲쵽�����ʯ��ˮ����ǡ�
����ʵ����ۣ�
����Ϊ����������ʵ����������жϳ����ɵĺ�ɫ����Ϊ��������
����Ϊ����������ʵ����������֤�����ɵĺ�ɫ����Ϊ��������������һ��ʵ�飺�ô���������ɫ���壬�����к�ɫ���屻�������������ǵó����ɵĺ�ɫ����Ϊ�������Ľ��ۡ�
����ͨ���÷�Ӧ��������϶����ǵĽ��������жϣ���ͨ��ʵ�����������ԣ�
����һ�������£�һ����̼���������ڼ��������£��ɷ������·�Ӧ��
CO +3Fe2O3 = 2Fe3O4+ CO2�� 4CO + Fe3O4 = Fe+ 4CO2��
������������(Fe3O4)Ϊ��ɫ���壬��ǿ���ԣ��ܹ�������������
�ס���ͬѧ�Ľ��� ______����Դ����۵������� ______��
����ʵ��̽��
�Է�Ӧ�����ɷ�������裺
����1����Ӧ�������ֻ��Fe��
����2����Ӧ�������ֻ��Fe3O4��
����3����Ӧ������� ______ ��
Ϊȷ��ʵ�����������еijɷ֣���ͬѧ�������ʵ�飬����������ѡ�Լ���������������ɸ�̽�����̣�������д�ڴ����Ӧλ�á�
��ѡ�Լ���������1mol/L CuSO4��0.01mol/L KSCN��Һ��1mol/L ���ᡢ0.01mol/L ��ˮ���Թܡ�����������ͷ�ιܡ�
ʵ����� | Ԥ������ͽ��� |
����һ��ȡӲ�ʲ������й�����������ֱ���A��B�Թ��У���������1mol/L CuSO4��Һ�������ܽ⡣ | ����A�Թ��к�ɫ���岻�ܽ⣬����û�й۲쵽�����������ɫ����Ϊ ______�� ����B�Թ����к�ɫ������������˵����ɫ�����к��� ______�� |
����������Թ�B����Һ���ˣ������ù���ϴ�Ӹɾ��������1mol/L����������ηֱ��������0.01mol/L��ˮ������0.01mol/L KSCN��Һ�� | ������Һ�����ɫ����______�� ������Һ���ɫ����______�� |
��������̽������ͬѧ��ͼͨ����Ӧǰ����������ı仯��ȷ����ɫ����ijɷ֣�����Ϊ������(�����������ڷ�Ӧ����ȫ��Ӧ)______(������������������)�������ǣ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����һ����ѧ�x��С�鴴����һ��ͨ��������⽫��������Ϊ��ѧ�ܵ�װ�á��������ƻ��ʵ������Ͷ�������Ϳ����������֮���ǿ�ͨ��H+�Ĺ���ۺ������ʡ���ṹ��ͼ��ʾ��������˵����ȷ����
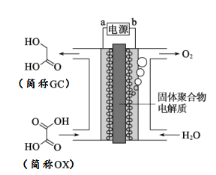
A. ��Դ��b��Ϊ����
B. ������ת�������У�����������H+�������������ƶ�
C. �����缫��ӦʽΪ��OX + 4H+ + 4e���T GC + H2O
D. Ϊ��ǿ�������Һ�����ԣ�����ˮ����������NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ҵ�����FeBr3�ϴ�������Һ���ɵõ���ı���Һ����ˮFeCl3�����������ܴﵽ��Ӧʵ��Ŀ�ĵ���(����)
A. 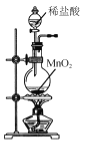 ��ȡCl2
��ȡCl2
B. 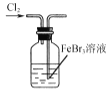 ʹBr��ת��ΪBr2
ʹBr��ת��ΪBr2
C.  ��Һ���ȷų�ˮ�㣬�ٵ�����ı���Һ
��Һ���ȷų�ˮ�㣬�ٵ�����ı���Һ
D.  ����Һ���ˮ�����ɻ����ˮFeCl3
����Һ���ˮ�����ɻ����ˮFeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ԫ�ػ�����Ļ�ѧ��������ȷ����
A.�����ӵĽṹʾ��ͼ��![]()
B.H��Cl�γɹ��ۼ��Ĺ��̣�![]()
C.Ǧ���طŵ�ʱ�ĸ�����Ӧ��Pb(s)��SO42��(aq)��2e��=PbSO4(s)
D.![]() ����
����![]() ���ɵ�����
���ɵ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡһ֧Ӳ�ʴ��Թܣ�ͨ���ű���ʳ��ˮ�ķ����Ⱥ��ռ����Թܼ���Ͱ��Թ������������ڹ�����(��ͼ)�����ж����Թ��ڷ����ķ�Ӧ�������˵����ȷ���ǣ� ��
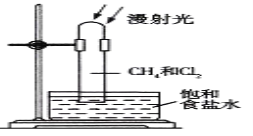
A. ��Ӧ�������Թ��ڻ���ɫ��dz���Թܱ������������
B. ����װ�÷��ںڰ�����![]() ��
��![]() Ҳ�ܷ�Ӧ
Ҳ�ܷ�Ӧ
C. �÷�Ӧ���õ�һ���л�����
D. ![]() ��
��![]() ��ȫ��Ӧ��Һ��������Һ������Թ�
��ȫ��Ӧ��Һ��������Һ������Թ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л���ı�ʾ�������ֶ����������dz��õ��л���ı�ʾ������
��![]() ��CH3CH2CH(CH3)CH3��CH4 ��
��CH3CH2CH(CH3)CH3��CH4 ��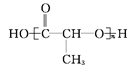 ��
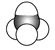
��
��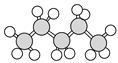 ��
��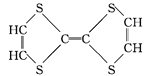 ��
��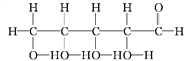
��1��������ʾ���������ڽṹ��ʽ����_______________(����ţ���ͬ)�����ڱ���ģ�͵���_______��
��2��д�����й����ŵ����ƣ�____________��____________��
��3��____________��____________��Ϊͬ���칹�塣
��1��д�������л���Ľṹ��ʽ��
��2��4����3�һ�����____________��
��2��2��ϩ____________��
��2��������������������
��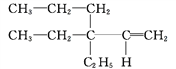 ____________��
____________��
��(CH3)3CCH(CH3)CH2CH3____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com