
1934年居里夫妇用α粒子(4He)轰击27Al得到一种自然界不存在的磷元素的一种同位素(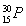 ):
):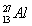 +
+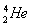 ―→
―→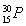 +
+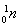 ,开创了人造核素的先河。下列有关说法不正确的是
,开创了人造核素的先河。下列有关说法不正确的是
A.该变化说明原子核在一般的化学反应中也能发生变化
B.该变化同样遵循质量守恒定律
C.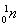 是一种电中性粒子
是一种电中性粒子
D.对于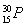 有:原子序数=质子数=中子数=核外电子数
有:原子序数=质子数=中子数=核外电子数
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源:2014年高一化学人教版必修二 1-1-2元素性质练习卷(解析版) 题型:选择题
下列关于碱金属的原子结构和性质的叙述中不正确的是( )
A.碱金属原子最外层都只有1个电子,在化学反应中容易失去最外层这个电子
B.都是强还原剂
C.都能在O2中燃烧生成过氧化物
D.都能与水反应生成强碱
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 模块水平检测1练习卷(解析版) 题型:实验题
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室制备乙酸乙酯的化学方程式:CH3COOH+C2H5OH CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
CH3COOC2H5+H2O,为证明浓硫酸在该反应中起到了催化剂和吸收剂的作用,某同学利用下图所示装置进行了以下四个实验,实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
实验编号试管Ⅰ中的试剂试管Ⅱ中试剂测得有机层的厚度/cm
A2 mL乙醇、2 mL乙酸、1 mL 18 mol·L-1浓硫酸饱和碳酸钠溶液5.0
B3 mL乙醇、2 mL乙酸0.1
C3 mL乙醇、2 mL乙酸、6mL 3 mol·L-1硫酸1.2
D3 mL乙醇、2 mL乙酸、盐酸1.2
(1)实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol/L。
(2)分析实验________(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。浓硫酸的吸水性能够提高乙酸乙酯产率的原因是_______________________________________________________________。
(3)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是____________________________________________(答出两条即可)。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 期中测试练习卷(解析版) 题型:填空题
(1)写出表示含有8个质子,10个中子的原子的化学符号________;
(2)已知阴离子aX2-和阳离子bYn+具有相同的核外电子排布,则a、b、n之间的关系为a=________;
(3)比较下列大小(填“>”或“<”)
A.原子半径:Cl______Na
B.酸性:H2CO3______H2SiO3
(4)某元素R气态氢化物的化学式为RH3,其最高价氧化物中含氧量为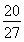 ,已知该元素的原子核中中子数和质子数相等,则该元素的名称是________。
,已知该元素的原子核中中子数和质子数相等,则该元素的名称是________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 期中测试练习卷(解析版) 题型:选择题
硫酸是一种重要的化工产品,2SO2+O2 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
A.只要选择适宜的条件,SO2和O2就能全部转化为SO3
B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零
C.如果反应前充入由18O原子组成的O2,反应达到平衡状态时,18O只存在于O2和SO3中
D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 4章化学与自然资源的开发利用练习卷(解析版) 题型:填空题
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
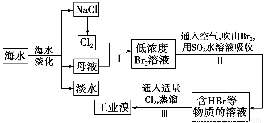
(1)请列举海水淡化的两种方法:________、________。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是_________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______,
由此反应可知,除环境保护外,在工业生产中应解决的主要问题是_______。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59 ℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:
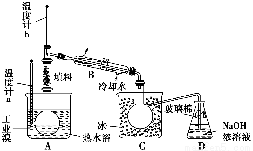
请你参与分析讨论:
①图中仪器B的名称是____________。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件?___________。
④C中液体颜色为________________。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 4章化学与自然资源的开发利用练习卷(解析版) 题型:选择题
下列有关聚乙烯的说法正确的是( )。
A.聚乙烯是通过加聚反应生成的
B.聚乙烯具有固定的元素组成,因而具有固定的熔、沸点
C.聚乙烯塑料袋因有毒,故不能装食品
D.聚乙烯因性质稳定,故不易造成污染
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 4.2资源综合利用环境保护练习卷(解析版) 题型:选择题
下图是实验室模拟煤的干馏的实验装置,下列叙述错误的是( )。
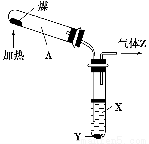
A.上图实验中发生了化学变化
B.液体X的pH>7,液体Y是黑色黏稠状的煤焦油
C.气体Z易燃,可还原CuO,也可使溴水褪色
D.液体Y是一种纯净物
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 3章有机化合物练习卷(解析版) 题型:填空题
化学式为C2H6O的化合物A具有如下性质:A+Na―→慢慢产生气泡
A+CH3COOH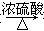 有香味的产物
有香味的产物
(1)根据上述信息,对该化合物可作出的判断是
( )。
A.一定含有—OH B.一定含有—COOH
C.A为乙醇 D.A为乙醛
(2)含A的体积分数为75%的水溶液可以用作______。
(3)A与钠反应的化学方程式:_____________。
(4)化合物A与CH3COOH反应生成的有香味的产物的结构简式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com