


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
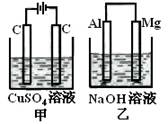
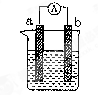
| A.相同条件下产生气体的体积:V甲=V乙 |
| B.溶液pH值变化:甲减小乙增大 |
| C.溶液的质量变化:甲减小乙增大 |
| D.电极反应式:甲中阴极:Cu2++2e—= Cu, 乙中负极:Mg - 2e—= Mg2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
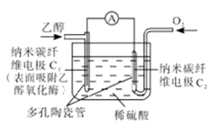
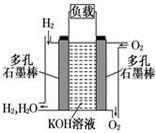
| A.O2在C2电极上得电子,被氧化 |
| B.电子由C2极经外电路流向C1极 |
| C.每转移6mole-,理论上生成22.4LCO2 |
| D.C1极的电极反应式为C2H5OH+3H2O-12e-=2CO2+12H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.装置①研究的是电解CuCl2溶液,b电极上有红色固体析出 |
| B.装置②研究的是金属的吸氧腐蚀,Fe上的反应为Fe-2e- = Fe2+ |
| C.装置③研究的是电解饱和食盐水, B电极发生的反应:2Cl--2e- = Cl2↑ |
| D.三个装置中涉及的主要反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

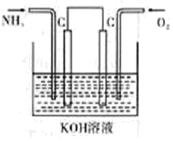
| A.该电池中镁为负极,发生还原反应 |
| B.电池工作时,OH-向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应为:Mg + ClO-+ H2O = Mg(OH)2↓+ Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com