
【题目】下列物质中,属于纯净物的是( )
①陶瓷 ②水泥 ③玻璃 ④漂白粉 ⑤胆矾 ⑥氯水 ⑦液氯
A. ①③⑤ B. ②④⑥ C. ⑤⑦ D. ⑥⑦
 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】下列化学方程式与基本反应类型都正确的是( )
A. CaO+H2O===Ca(OH)2 化合反应
B. 2KClO3===2KCl+3O2↑ 分解反应
C. CuO+CO![]() Cu+CO2 置换反应
Cu+CO2 置换反应
D. 2KOH+Na2CO3===K2CO3+2NaOH 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
已知A是芳香烃,苯环上只有一个取代基,A完全加氢后分子中有两个甲基,E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色,其可以用来合成新型药物H,合成路线如图所示。

已知:

请回答下列问题:
(1)写出有机物A的结构简式:____________。有机物D中存在的官能团名称为_______________。
(2)上述反应过程中属于取代反应的有________________(填序号)。
(3)有机物H在一定条件下可以聚合形成高分子,写出该聚合物的结构简式:_______________________。
(4)写出H在氢氧化钠催化作用下的水解方程式:_________________________。
(5)有机物E有多种同分异构体,写出符合下列条件的同分异构体的结构简式:_________________。
a.存在苯环且苯环上核磁共振氢谱只有2组峰值
b.与新制Cu(OH)2悬浊液作用产生砖红色沉淀
c.加入FeCl3溶液显色
(6)参照H的上述合成路线,设计一条由石油产品和NH2—CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线:___________________________________________________________________(需注明反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是
A. 碳酸钠的水解反应:CO32-+ H3O+![]() HCO3-+ H2O
HCO3-+ H2O
B. 氢氧化铁胶体的制备:Fe3+ + 3OH-=Fe(OH)3(胶体)
C. 偏铝酸钠中滴加碳酸氢钠溶液: AlO2- +HCO3- +H2O= Al(OH)3↓ + CO32-
D. 碱性氢氧燃料电池的正极反应式:4OH--4e-=2H2O + O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。

(一)硫化物(FexSy)的组成
实验步骤:
步骤Ⅰ 如图连接装置,检査装置气密性,装入药品;
步骤Ⅱ 打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2
步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
……
请回答:
⑴仪器a的作用为______________________。
(2)步骤Ⅲ中,停止加热后还需继续通入一段时间的O2,其目的为__________________。
(3)步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___________________。
(4)取25. 00 mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为___________________。
(5)问题讨论:有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案________(填“是”或“否”)合理,原因为_______________________。
(二)探究反应后D装置所得溶液中含硫化合物的组成。
理论推测:溶液中除含有Na2SO4外,还可能含有Na2SO3。
实验探究:滴定法测定溶液中Na2SO3的含量。
可供选择的试剂:①0.10 mol L-1 KmnO4酸性溶液 ②30%H2O2
③0.10 mol L-1 KI淀粉溶液
(6)所选试剂为___________(填序号);所选试剂应装在_____________(填“酸式”或“碱式”)滴定管中。
⑦所利用的反应原理为__________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以提取溴,主要反应为: 2Br Cl2 Br2 2Cl,下列说法正确的是( )
A. 溴离子具有氧化性 B. 氯气是还原剂
C. 该反应属于复分解反应 D. 氯气的氧化性比溴单质强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7是一种橙红色固体,可用于火柴制造、电镀、有机合成等方面。用某酸性废液(主要含Cr3+、还含有少量Fe2+、Fe3+和Al3+等)制备的流程如下:
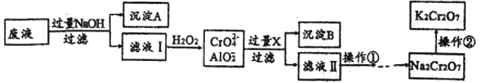
已知:H++CrO2-+H2O![]() Cr(OH)3
Cr(OH)3![]() Cr3++3OH-
Cr3++3OH-
回答下列问题:
(1)沉淀A的主要成分是_____________(填化学式,下同),流程中的X是__________。
(2)滤液Ⅰ中铬元素的存在形式主要是_____________(填离子符号)。
(3)操作是向滤液中加入稀硫酸调PH至一定范围。在酸性环境中CrO42-转化为Cr2O72-,溶液变为橙红色,该转化的离子方程式是__________;若PH高于此范围,造成的影响是__________。
(4)操作②是向Na2Cr2O7溶液中加入KCl固体后得到K2Cr2O7,说明相同温度下,在水中的溶解度:Na2Cr2O7______________ K2Cr2O7(填“>”、“<”或“=”)。
(5)PbO2可直接将溶液中的Cr3+氧化成Cr2O72-,该反应的离子方程式是__________。
(6)K2Cr2O7可用来测定溶液中Fe2+的含量,还原产物为Cr3+。若1L FeSO4溶液与100mL 0.1mol/L K2Cr2O7溶液恰好完全反应,则c(FeSO4)=___________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 氯气和澄清石灰水反应:Cl2+2OH-=Cl-+ClO-+H2O
B. 碳酸氢钠溶液与氢氧化钠溶液反应:OH-+HCO3-=CO2+H2O
C. 向氯化铝溶液中加入过量的氨水:Al3++3OH-=Al(OH)3↓
D. 用大理石和稀醋酸的反应:CaCO3+2H+=Ca2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)在溶液中对生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=﹣lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是

A. HClO2的电离平衡常数的数值Ka=10-8
B. pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH-
C. pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com