
【题目】氮的氧化物(NOx)是大气污染物之一。工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),常见处理法有:
(1)可用氨催化吸收法处理NOx,反应原理如下:4xNH3+6NOx![]() (2x+3)N2+6xH2O
(2x+3)N2+6xH2O
某化学兴趣小组模拟该处理过程的实验装置如下:
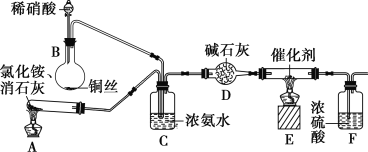
①装置A中发生反应的化学方程式为________________________________。
②装置D中碱石灰的作用是____________________。
(2)用Na2CO3溶液吸收法处理NOx。已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3===2NaNO2+CO2 (Ⅰ)
2NO2+Na2CO3===NaNO2+NaNO3+CO2 (Ⅱ)
①当NOx被Na2CO3溶液完全吸收时,x的值不可能是________(填字母)。
A.1.9 B.1.7 C.1.5 D.1.3
②用足量的Na2CO3溶液完全吸收NOx,每产生22.4 L(标准状况)CO2(全部逸出)时,吸收液质量就增加44 g,则NOx中的x值为________________。
【答案】(1)①2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O②除去气体中含有的水蒸气
CaCl2+2NH3↑+2H2O②除去气体中含有的水蒸气
(2)①D②15/8(或1.875)
【解析】
试题分析:(1)①氯化铵与消石灰反应生成氯化钙、氨气和水,反应的化学方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;②装置D中碱石灰的作用是为了除去气体中含有的水蒸气。
CaCl2+2NH3↑+2H2O;②装置D中碱石灰的作用是为了除去气体中含有的水蒸气。
(2)①由方程式可知,NO单独不能被吸收,NO和NO2混合气体被NaOH溶液被完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,x最小值为2+1/2=1.5,因为混有NO,所以x最大值<2,x的取值范围为1.5≤x<2,答案选D;
②设由NO2与纯碱反应产生的CO2为a mol,由NO和NO2与纯碱反应产生的CO2为b mol,
2NO2+Na2CO3===NaNO2+NaNO3+CO2 △m = 48g
a 48a
NO+NO2+Na2CO3===2NaNO2+CO2 △m = 32g
b 32b
a+b=1,48a+32b=44,解得 a=0.75mol、b=0.25mol,n(NO2) = 0.75mol×2+0.25mol=1.75mol,n(NO) = 0.25mol,x=![]()
![]() =1.875。
=1.875。


科目:高中化学 来源: 题型:
【题目】下列实验操作不正确的是
A. 用量筒量取25 mL蒸馏水 B. 用分液漏斗分离乙醇和水
C. 用烧杯溶解FeCl3试样 D. 用托盘天平称量NaCl固体5.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列结构的物质:①CH3(CH2)3CH3
②CH3CH2CH2CH2CH3
③CH3CH2CH2CH2CH2CH3
④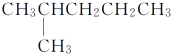
⑤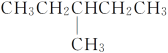
⑥
⑦
其中,属于同系物的是________;属于同分异构体的是__________;属于同种物质的是________。
A①② B②③ C③④⑤⑥⑦ D①③ E③④⑤⑦ F④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为0.1mol·L-1的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是 ( )
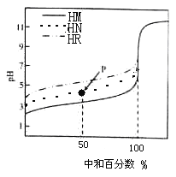
A.三种酸的电离常数关系:KHM>KHN>KHR
B.pH=7时,三种溶液中:c(M-)>c(N-)>c(R-)
C.滴定至P点时,溶液中:c(Na+)> c(N-)>c(HN)>c(H+)>c(OH-)
D.当中和百分数达100%时,将三种溶液混合后: c(HM)+c(HN)+c(HR)=c(OH-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列无色澄清的溶液中,可能大量共存的离子组是( )
A. Cl-、SO32-、Fe2+、H+ B. NH4+、Al3+、NO3-、HCO3-
C. Na+、K+、OH-、AlO2- D. K+、Na+、SO42-、MnO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示(夹持仪器已略去)。
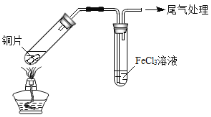
A B
(1)实验前,应先检查装置的 ;实验中产生的尾气应通入 溶液。
(2)实验过程中需要配制100mL1mol/L FeCl3溶液(未用浓盐酸酸化),所需要的玻璃仪器有:烧杯、量筒、胶头滴管、玻璃棒、 。
(3)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A。 |
写出装置A中产生SO2的化学方程式: 。
(4)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因(用化学用语解释): 。
写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式: 。
(5)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。
步骤② | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
步骤③ | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
⑹综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III. 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活中常见的有机物和基本营养物质叙述正确的是
①吃馒头,多咀嚼后有甜味属于水解反应
②油脂是多种高级脂肪酸的甘油酯
③油脂都不能使溴水和酸性KMnO4溶液褪色
④天然蛋白质水解的最终产物均为α氨基酸
A. ①②③ B. ①②④ C. ②③ ④ D. ①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com