
【题目】请同学们根据官能团的不同对下列有机物进行分类(填序号).
①CH3CH2OH② ![]() ③CH3CH2Br④
③CH3CH2Br④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]() ⑦
⑦ ![]() ⑧
⑧ ![]() ⑨
⑨ ![]() ⑩
⑩ 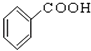
(1)卤代烃:;
(2)酯:;
(3)醇:;
(4)醛:;
(5)羧酸 .
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.加碘食盐中的含碘物质为碘单质B.聚氯乙烯塑料品常用于食品包装
C.苯应密封保存,置于阴凉处且远离火源D.无水乙醇常用于杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.油脂都不能使溴的四氯化碳溶液褪色
D.液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的乙醇在氧气不足的情况下燃烧,得到CO2、CO和 H2O的总质量为27.6g,其中H2O的质量为10.8g,则CO的质量是( )
A.1.4 g
B.2.2 g
C.4.4 g
D.在2.2 g和4.4 g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式
6C(s)+5H2(g)+3N2(g)+9O2(g) 2C3H5(ONO2)3(l) ΔH1
2 H2(g)+ O2(g) 2H2O(g) ΔH2
C(s)+ O2(g) CO2(g) ΔH3
则反应4C3H5(ONO2)3(l) 12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
A. 12ΔH3+5ΔH2-2ΔH1 B. 2ΔH1-5ΔH2-12ΔH3
C. 12ΔH3-5ΔH2-2ΔH1 D. ΔH1-5ΔH2-12ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为t℃时,在10mL1.0 mol·L-1的盐酸中,逐滴滴入x mol·L-1的氨水,随着氨水逐渐加入,溶液中的pH变化曲线如图所示(忽略混合时溶液体积的变化,c点时溶液的温度为常温)。则下列有关判断正确的是

A. b点,c(NH4+)>c(Cl-)>c(H+)>c(OH-)
B. a点,水的电离程度最大
C. x=1.0
D. c点时,c(NH3·H2O)=0.5(x-1) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品。在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙。发生反应:
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s) ![]() CaWO4(s)+2OHˉ(aq) K1
CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表,请回答下列问题:
温度/℃ | 25 | 50 | 90 | 100 |
K1 | 79.96 | 208.06 | 222.88 | 258.05 |
(1)判断反应Ⅰ的△S ______0、△H______0(填“>”、“=”或“<”),在______(填“较高”或“较低”)温度下有利于该反应自发进行。
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小。它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)![]() Ca2+(aq) + WO42ˉ(aq) K2
Ca2+(aq) + WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s)![]() Ca2+(aq) + 2OHˉ(aq) K3
Ca2+(aq) + 2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=______(用K2、K3表示)。
②根据反应Ⅱ,右图为不同温度下CaWO4的沉淀溶解平衡曲线。则T1 ____T2(填“>”“=”或“<”)。T1时,向0.5 molLˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=_______molLˉ1。(假设反应前后体积不变)

(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率。反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3。
①在反应混合液中不直接通入CO2,其理由是_____________;
②用平衡移动原理解释添加酸性物质的理由______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐,易溶于水,微溶于乙醇。某化学兴趣小组对亚硝酸钠与硫酸反应的气体产物成分及NaNO2性质进行如下探究:

已知:①NO+NO2+2OH-=2NO2-+H2O;
②气体液化的温度:NO2:21℃,NO:152℃。
(1)仪器a的名称是_____________________。
(2)若要验证A中反应生成的气体产物成分且又不能污染环境,仪器的连接顺序为(用字母序号从左→右表示):A、C、______、______、__________。
(3)B中NaOH溶液的作用是_____________________________________。
(4)反应前打开弹簧夹,通入一段时间氮气,其目的是_______________________;关闭弹簧夹,打开分液漏斗活寒,滴入70%硫酸后,A中产生红棕色气体。
(5)①确认A反应产生的气体中含有NO的现象是:_________________________。
②A中反应的化学反应方程式为________________________________。
(6)利用所提供的试剂(NaNO2溶液、KMnO4溶液、KI溶液、稀硫酸、淀粉溶液)设计实验,证明酸性条件下NaNO2具有氧化性________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 形成离子键的阴阳离子间只存在静电吸引力
B. HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
C. 第三周期非金属元素含氧酸的酸性从左到右依次增强
D. 只要含有离子键的化合物就是离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com