
| A. | (a+1.25) | B. | (a+9.6 )g | C. | (a+5.1)g | D. | 无法确定 |
分析 铜、铁先被硝酸氧化,向所得到溶液中加入KSCN溶液无明显变化,说明铁反应生成硝酸亚铁,然后生成气体又被O2氧化成硝酸,所以可以直接认为ag铜、铁失的电子被1.68LO2获得,由于没有生成三价铁,所以铜和铁都是失2个电子,根据电荷守恒可得金属失去电子物质的量等于氢氧根离子的物质的量,沉淀质量为金属质量以氢氧根离子质量之和.
解答 解:铜、铁先被硝酸氧化,向所得到溶液中加入KSCN溶液无明显变化,说明铁反应生成硝酸亚铁,然后生成气体又被O2氧化成硝酸,所以可以直接认为ag铜、铁失的电子被1.68LO2获得,根据电子转移守恒,故金属失去的电子为:$\frac{1.68L}{22.4L/mol}$×4=0.3mol,
根据电荷守恒可得金属失去电子物质的量等于氢氧根离子的物质的量=0.3mol,
则生成沉淀质量为:ag+0.3mol×17g/mol=(a+5.1)g,
故选C.
点评 本题考查混合物反应计算、氧化还原反应计算,题目难度中等,利用常规方无法解答,是守恒思想在混合计算典型利用,判断金属失去的电子等于氧气获得的电子是关键.


 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:选择题
| A. | 碘化氢的生成速率大于其分解速率 | |
| B. | 碘化氢的生成速率等于其分解速率 | |
| C. | 加催化剂不会影响达到平衡的时间 | |
| D. | 升高温度可以缩短到达平衡状态的时间 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
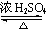 CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式
CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式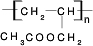 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
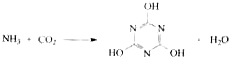 下列有关三聚氰胺的说法正确的是( )
下列有关三聚氰胺的说法正确的是( )| A. | 分子式为C3H6N3O3 | B. | 分子中既含极性键,又含非极性键 | ||
| C. | 属于共价化合物 | D. | 生成该物质的上述反应为中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑥>⑤>④>①>③>② | B. | ⑥>④>⑤>①>③>② | C. | ⑥>④>⑤>①>②>③ | D. | ⑥>⑤>④>①>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上10月月考化学试卷(解析版) 题型:选择题
已知下列两个气态物质之间的反应:
C2H2(g)+H2(g)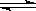 C2H4(g)①
C2H4(g)①
2CH4(g)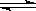 C2H4(g)+2H2(g)②
C2H4(g)+2H2(g)②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
(Q1、Q2、Q3均为正值)
C(s)+2H2(g)=CH4(g)ΔH=-Q1
2C(s)+H2(g)=C2H2(g)ΔH=-Q2
2C(s)+2H2(g)=C2H4(g)ΔH=-Q3Q值大小比较正确的是( )
A. Q1>Q3>Q2 B. Q1>Q2>Q3 C. Q2>Q1>Q3 D. Q3>Q1>Q2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com