

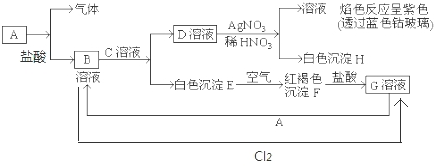
分析 白色沉淀E在空气中转化为红褐色沉淀F,则E为Fe(OH)2,F为Fe(OH)3,F与盐酸反应得到G,G与单质A反应得到B,结合转化关系及元素守恒可知,A为Fe,G为FeCl3,B为FeCl2,B与C溶液反应得到D,D与AgNO3生成白色沉淀H,可知H为AgCl,透过蓝色钴玻璃观察焰色反应为紫色,可知D溶液中含有K+,故D为KCl,C为KOH,金属Fe与稀盐酸反应会生成FeCl2和气体H2.
解答 解:白色沉淀E在空气中转化为红褐色沉淀F,则E为Fe(OH)2,F为Fe(OH)3,F与盐酸反应得到G,G与单质A反应得到B,结合转化关系及元素守恒可知,A为Fe,G为FeCl3,B为FeCl2,B与C溶液反应得到D,D与AgNO3生成白色沉淀H,可知H为AgCl,透过蓝色钴玻璃观察焰色反应为紫色,可知D溶液中含有K+,故D为KCl,C为KOH,金属Fe与稀盐酸反应会生成FeCl2和气体H2.
(1)由上述分析可知,B为FeCl2,D为KCl,故答案为:FeCl2;KCl;
(2)Fe(OH)2在空气中与O2反应转变为Fe(OH)3,反应为4Fe(OH)2+2H2O+O2=4Fe(OH)3,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(3)FeCl3溶液中加入铜粉反应的离子方程式:2Fe3++Cu═2Fe2++Cu2+,
故答案为:2Fe3++Cu═2Fe2++Cu2+.
点评 本题考查无机物的推断,E到F的颜色变化及焰色反应等时推断突破口,侧重铁及其化合物的性质及转化的考查,题目难度不大.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2中混有少量HCl:通过盛有足量硝酸银溶液的洗气瓶洗气 | |
| B. | Cl2中混有少量水蒸气:先通过足量浓硫酸,再用向下排空气法收集氯气 | |
| C. | HCl中混有少量Cl2:通过盛有四氯化碳的洗气瓶洗气 | |
| D. | HCl中混有少量Cl2:通入足量氢气并光照 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学式 | CH3COOH | HA | HNO2 | H2CO3 |
| Ka | Ka=1.8×10-5 | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{2a-4b}{V}$ | B. | $\frac{2(a-b)}{V}$ | C. | $\frac{a-2b}{V}$ | D. | $\frac{2a-b}{V}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溶解后过滤的方法除去CaCl2中的少量的ZnSO4 | |
| B. | 用萃取的方法分离NaCl溶液和汽油 | |
| C. | 用酒精萃取碘水中的碘 | |
| D. | 用蒸馏的方法除去水中的不挥发的杂质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com