
| A. | Fe2O3固体中加入HI溶液:Fe2O3+6H+═2Fe3++3H2O | |
| B. | NaAlO2溶液和NaHCO3溶液混合:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | |
| C. | 碳酸氢钙溶液中加入少量澄清石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O | |
| D. | NaOH和Ba(OH)2混合溶液中通入少量CO2:2OH-+CO2═CO32-+H2O |
分析 A.铁离子具有强氧化性,能够氧化碘离子;
B.NaAlO2溶液和NaHCO3溶液混合反应生成氢氧化铝和碳酸根离子;
C.碳酸氢钙溶液中加入少量澄清石灰水生成碳酸钙和水;
D.NaOH和Ba(OH)2混合溶液中通入少量CO2反应生成碳酸钙沉淀.
解答 解:A.铁离子具有强氧化性,能够氧化碘离子,正确的离子方程式为:Fe2O3+6H++2I-=2Fe2++I2+3H2O,故A错误;
B.NaAlO2溶液和NaHCO3溶液混合反应生成氢氧化铝和碳酸根离子,反应的离子方程式为:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32-,故B正确;
C.碳酸氢钙溶液中加入少量澄清石灰水生成碳酸钙和水,反应的离子方程式为:Ca2++OH-+HCO3-═CaCO3↓+H2O,故C错误;
D.NaOH和Ba(OH)2混合溶液中通入少量CO2反应生成碳酸钙沉淀,反应的离子方程式为:Ba2++2OH-+CO2═BaCO3↓+H2O,故D错误.
故选B.
点评 本题考查了离子方程式的书写方法,题目难度中等,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:选择题
| A. | Cl2水,NaOH(aq) | B. | KMnO4(aq),氨水 | C. | H2O2溶液,氧化铜 | D. | HNO3(aq),氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②⑤⑥⑧ | C. | ②⑦⑧ | D. | ③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.2g甲酸中,所含化学键的数目为0.8 NA | |
| B. | 常温下,28g Fe与足量的浓硝酸反应,转移的电子数为1.5NA | |
| C. | 标准状况下,2.24LNH3和CH4的混合气体,所含电子总数为NA | |
| D. | 标准状况下,22.4L己烷所含有的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | d1>d2 | C. | bω2≥aω1 | D. | a d1ω1=b d2ω2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
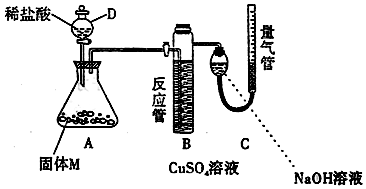
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大量使用含磷洗涤剂会引发潮汐 | |
| B. | 减少使用氟氯代烃的目的是减少酸雨 | |
| C. | 大量开采地下水,矿产资源,以满足社会经济发展的需求 | |
| D. | 氢燃料电池汽车的使用,可以有效减少城市空气污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL pH=13的氨水与10mL pH=l的盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | l0 mL0.1 mol/L NH4Cl溶液与5mL 0.2mol/LNaOH溶液混合:c(Cl-)=c(Na+)>c(OH-)>(H+) | |
| C. | 10 mL 0.1 mol/L CH3COOH溶液与10 mL pH=13的NaOH溶液混合:c(CH3COO-)=c(Na+)>c(OH-)>c(H+) | |
| D. | l0 mL 0.5mol/L CH3COONa溶液与6mL pH=0的盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )
常温下,向100mL 0.01mol•L-1的HA溶液中逐滴加入0.02mol•L-1的MOH溶液,图中所示曲线表示混合溶液的pH的变化情况,下列说法正确的是( )| A. | HA为弱酸 | |
| B. | 常温下,MA溶液的pH>7 | |
| C. | K点对应的溶液中:c(M+)+c(MOH)=c(A-) | |
| D. | 在N到K间任意一点对应的溶液中:c(M+)+c(H+)=c(OH-)+c(A-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com