
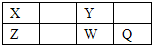
 短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )
短周期元素X、Y、Z、W、Q在元素周期表的位置如表所示,其中X元素的原子内层电子数是最外层电子数的一半,则下列说法不正确的是( )| A、钠与W可能形成Na2W2化合物 |
| B、由X与Q两种元素组成的物质在熔融时不能导电 |
| C、X和Z的单质均有原子晶体 |
| D、X有多种同素异形体,而Y不存在同素异形体 |


科目:高中化学 来源: 题型:
| A、0﹒5mo1C2H4 |
| B、11﹒2L(标准状况)C2H2 |
| C、含6﹒02×1023个氢原子的CH4 |
| D、18g H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
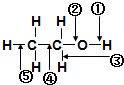
| A、和金属钠作用时,键①断裂 |
| B、和浓硫酸共热至170℃时,键②和⑤断裂 |
| C、和浓硫酸共热至140℃时,键②和③断裂 |
| D、在铜催化下和氧气反应时,键①和③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此时水的离子积KW=1.0×10-14 |
| B、水电离出的c(H+)=1.0×10-10mol/L |
| C、水的电离度程不随温度升高而变化 |
| D、100℃时,蒸馏水呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况时,22.4L四氯化碳所含有的分子数为NA |
| B、34g H2O2中含有的非极性共价键数为 NA |
| C、碱性锌锰电池中,当有1.3g的锌消耗,则转移的电子数为0.002NA |
| D、将16gO2与64gSO2在一定的条件下充分反应生成的SO3分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、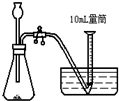 |
B、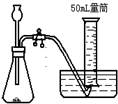 |
C、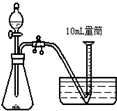 |
D、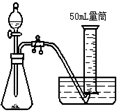 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4 |
| B、C2H6 |
| C、C3H8 |
| D、C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中溶质是Na2CO3和NaOH |
| B、溶液中的离子浓度:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| C、溶液中的离子浓度:c(Na+)>c(HCO3-)=c(CO32-)>c(OH-)>c(H+) |
| D、溶液中的离子浓度:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com