
【题目】分子式为C5H12O且可与金属钠反应放出氢气的有机化合物有(不考虑立体异构)( )
A.5种 B.6种 C.7种 D.8种
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)金刚石和石墨燃烧反应中的能量变化如图a所示。

在通常状况下,金刚石和石墨中, (填“金刚石”或“石墨”)更稳定,石墨的燃烧热△H= kJ·mol-1。
(2)采用电化学法可将甲烷转化为二氧化碳,试写出以氢氧化钾水溶液作电解质时,该电池正极反应方程式 。
(3)CO2为原料还可合成多种物质。工业上常以CO2(g)与H2(g)为原料合成乙醇。①2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(l) 该反应物的总能量大于生成物的总能量,则该反应的△H= (填“>0”、“<0”、“=0”或“不能确定”)
CH3CH2OH(g)+3H2O(l) 该反应物的总能量大于生成物的总能量,则该反应的△H= (填“>0”、“<0”、“=0”或“不能确定”)
②下图是一种以烟道气为原料合成乙醇的工作原理示意图。
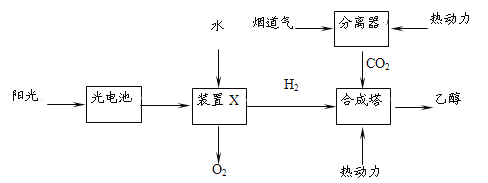
对上述流程的分析,下列说法正确的是 。
A.该流程至少包含4种形式的能量转化
B.流程设计体现了绿色化学思想
C.合成塔中生成乙醇的反应是化合反应
③图b所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。该电池负极的电极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途。
(1)砷元素的基态原子价电子排布图为______________。
(2)汽车安全气囊的产生药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质,在NaN3固体中阴离子的立体构型______________。
(3)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O,产物中的H[AuCl4]是配合物,它的配位体是______________,发生电离的方程式为______________
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明是节能减排的有效举措,已知砷化镓的晶胞结构如图,晶胞棱长为apm。
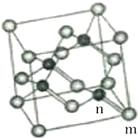
①砷化镓的化学式______________,镓原子的配位数为______________。
②砷化镓的晶胞中m位置Ga原子与n位置As原子之间的距离为________pm (用含“a”的表达式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:
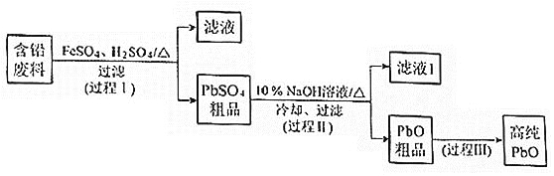
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__________。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42=2Fe3++PbSO4+2H2O
ii: ……
①写出ii的离子方程式:________________。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.______________。
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)![]() NaHPbO2(aq),其溶解度曲线如图所示。
NaHPbO2(aq),其溶解度曲线如图所示。
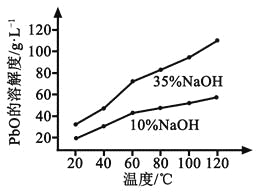
①过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是____._(选填序号)。
A.减少PbO的损失,提高产品的产率
B.重复利用氢氧化钠,提高原料的利用率
C.增加Na2SO4浓度,提高脱硫效率
②过滤Ⅲ的目的是提纯,综合上述溶解度曲线,简述过程Ⅲ的操作_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图只表示出与反应有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请填写下列空白。

(1)化合物W可能是________或__________(填化学式),C的结构式是________,
(2)D的组成元素在周期表中的位置是__________。
(3)反应③的离子方程式:________________________。
(4)已知G的极稀溶液被锌还原为NH4NO3,试写出G与锌反应的化学方程式: __________________。
(5)足量的铜与浓度均为2 mol/L的G和H2SO4的混合溶液100 mL充分反应后,转移的电子数为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于溶液和胶体的叙述,正确的是( )
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物分子中含有n个—CH2—,m个—CH—,a个—CH3,其余为—OH,则分子中—OH的个数为
A.2n+3m-a B.n+m+a C.m+2-a D.m+2n+2-a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸480mL。
(1)选用的主要玻璃仪器有:
①_______,②_______,③_______,④______,⑤________。
(2)简要回答下列问题:所需浓硫酸的体积为_______mL(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中,在一定条件下发生反应:2A(?)![]() B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
B (g)+C(s),且达到平衡,当升高温度时,容器内气体的密度变大,则下列判断错误的是
A. 若正反应为吸热反应,则A为非气态
B. 若正反应为放热反应,则A为气态
C. 若在平衡体系中加入少量C,则该平衡不移动
D. 压强对该平衡的移动无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com