
【题目】镁、硼及其化合物在工农业生产中应用广泛。已知:硼、铝同主族;硼砂常指四硼酸钠的十水合物,化学式为Na2B4O7·10H2O。利用硼镁矿(主要成分为Mg2B2O5·H2O)制取金属镁及粗硼的工艺流程图如图所示:

(1)Mg2B2O5·H2O 中B的化合价为______价。
(2)操作②的主要步骤是_______________和过滤,从而获得MgCl26H2O。
(3)MgCl26H2O在HCl氛围中加热才能制得无水氯化镁。其原因是________________;若用情性电极电解MgCl2溶液,其阴极反应式为_____________________________。
(4)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3制取H3BO3晶体,该反应的离子方程式为______;X为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方裎式为_____________。
(5)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+=Mg2++2H2O。常温下,若起始电解质溶液pH=1,则当pH =2时,溶液中Mg2+的浓度为___________。
【答案】 +3 加热浓缩、冷却结晶 抑制MgCl2水解 2H2O+2e-+Mg2+=H2↑+Mg(OH)2↓ B4O72-+2H++5H2O=4H3BO3 3Mg+B2O3![]() 2B+3MgO 0.045mol/L
2B+3MgO 0.045mol/L
【解析】(1)Mg元素化合价为+2价,氧元素化合价-2价,依据化合价代数和为0计算可得到硼元素化合价为+3价。(2)从溶液中得到结晶水合物为防止失去结晶水,不能直接蒸发结晶,应采用蒸发浓缩、冷却结晶的方法。(3)MgCl2是强酸弱碱盐,水解显酸性,加热会促进Mg2+水解,在HCl氛围中加热,可抑制MgCl2水解;情性电极电解MgCl2溶液,阴极上由水电离的H+得电子发生还原反应生成H2,同时Mg2+会结合OH-生成沉淀,因此阴极的电极反应式为:2H2O+2e-+Mg2+=H2↑+Mg(OH)2↓。(4)由化学式可知,硼砂溶于90℃热水后,用稀硫酸调pH至2~3制取H3BO3,B的化合价并没有发生变化,根据原子守恒和电荷守恒可知反应的离子方程式为:B4O72-+2H++5H2O=4H3BO3;X为H3BO3晶体加热脱水的产物,则为B2O3,与Mg反应生成粗硼和氧化镁,反应的化学方程式为3Mg+B2O3![]() 2B+3MgO。(5)若起始pH=1,则pH=2时溶液中,氢离子浓度减小0.1molL-1-0.01 molL-1=0.09 molL-1,依据总反应式Mg+H2O2+2H+=Mg2++2H2O可得c(Mg2+)=0.045 molL-1。
2B+3MgO。(5)若起始pH=1,则pH=2时溶液中,氢离子浓度减小0.1molL-1-0.01 molL-1=0.09 molL-1,依据总反应式Mg+H2O2+2H+=Mg2++2H2O可得c(Mg2+)=0.045 molL-1。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学为了检验纤维素的水解产物是否为葡萄糖,他将纤维素与70%的硫酸共热后加入新制Cu(OH)2悬浊液并加热煮沸,无红色沉淀生成,以下解释正确的是( )
A. 纤维素水解产物中无葡萄糖
B. 使用的硫酸过浓只发生了脱水反应
C. 由于水解产物与硫酸共存所以见不到红色沉淀
D. 加热时间不够长,所以见不到红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
![]()
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应.下列判断正确的是(不考虑NO2转化为N2O4)
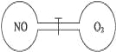
A.开始时左右两室分子数相同
B.反应前后NO室压强相同
C.最终容器内密度与原来相同
D.最终容器内无O2存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理的有关知识回答下列问题:
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)=SiO2 △H=-989.2 kJ·mol-1,有关键能数据如下表:
化学键 | Si-O | O=O | Si-Si |
键能kJ·mol-1 | X | 498.8 | 176 |
则X的值为_________。
(2)加热N2O5,依次发生的分解反应为①N2O5![]() N2O3+O2,②N2O3
N2O3+O2,②N2O3![]() N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为_________。
N2O+O2,在1 L密闭容器中充入4 mol N2O5,加热到t ℃,达到平衡状态后O2的平衡浓度为4.5 mol/L,N2O3的平衡浓度为1.7 mol/L,则t℃时反应①的平衡常数为_________。
(3)一只规格为amL的滴定管,其尖嘴部分充满溶液,管内液面在mmL处,当液面降到n mL处时,下列判断正确的是_________。
A.流出溶液的体积为(m-n)mL B.流出溶液的体积为(n-m)mL
C.管内溶液体积等于(a-n)mL D.管内溶液体积多于nmL
(4)已知某二元酸(H2A)溶液按下式发生一级和二级电离:H2A=H++HA-;HA-![]() H++A2-,且0.1mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是_________0.11 mol·L-1(填“<”“>”或“=”),理由是__________。
H++A2-,且0.1mol·L-1的NaHA溶液的pH=2,则0.1mol·L-1的H2A溶液中氢离子的物质的量浓度可能是_________0.11 mol·L-1(填“<”“>”或“=”),理由是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A,B,C,D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10.A与C同主族,B与D同主族,A,C原子的最外层电子数之和等于B原子的次外层电子数.则下列叙述正确的是( )
A.D元素处于元素周期表中第3周期VIA族
B.四种元素的原子半径:A<B<C<D
C.B,D的最高价氧化物具有相似的物理性质和化学性质
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( ) 
A.该反应是吸热反应
B.断裂1molA﹣A键和1molB﹣B键可放出xkJ能量
C.断裂2molA﹣B键需要吸收ykJ能量
D.2molAB的总能量高于1molA2和1molB2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组一定不能大量共存的是( )
A.K+ 、Na+、CO32-、NO3-B.NH4+、HCO3-、NO3-、Na+
C.Al3+、HCO3-、NO3-、Cl -D.SiO32-、Na+、K+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的同位素 ![]() ,已知M=30,且M﹣Z=16,则:
,已知M=30,且M﹣Z=16,则:
(1)X元素为 .
(2)X的气态氢化物电子式 .
(3)X单质与强碱溶液反应的化学方程式 .
(4)X的氧化物与酸反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com