
| A. | 在蒸馏水中滴加浓H2SO4,Kw不变 | |
| B. | CaCO3不易溶于稀硫酸,也不易溶于醋酸 | |
| C. | NaCI溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| D. | 在Na2S稀溶液中,c(H+)=c( OH-)-2c(H2S)-c(HS-) |
分析 A.温度不变Kw不变,浓硫酸溶解于水放热;
B.碳酸钙和硫酸反应生成硫酸钙微溶于水附着表面阻止反应进行,碳酸酸性弱于硝酸,碳酸钙可以溶解于醋酸;
C.NaCI溶液中钠离子和氯离子不水解,醋酸铵溶液中醋酸根离子和铵根离子水解相互促进,促进水的电离;
D.在Na2S稀溶液中中 存在质子守恒,水电离出所有氢氧根离子和氢离子存在形式总和相同;
解答 A.在蒸馏水中滴加浓H2SO4,溶液温度升高,Kw发生变化,故A错误;
B.碳酸钙和硫酸反应生成硫酸钙微溶于水附着表面阻止反应进行,CaCO3不易溶于稀硫酸,碳酸酸性弱于醋酸,碳酸钙可以溶解于醋酸,故B错误;
C.NaCI溶液和CH3COONH4溶液均显中性,氯化钠是强酸强碱盐不水解,醋酸铵溶液中醋酸根离子和铵根离子水解促进水的电离,相互促进程度相近溶液呈中性,两溶液中水的电离程度不相同,故C错误;
D.在Na2S稀溶液中存在质子守恒,c( OH-)=c(H+)+2c(H2S)+c(HS-),则得到c(H+)=c( OH-)-2c(H2S)-c(HS-),故D正确;
故选D.
点评 本题考查了电解质溶液中离子积常数,盐类水解原理,电解质溶液中质子守恒等知识点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 钢是用量最大、用途最广的合金,根据其化学成分可分为高碳钢和低碳钢两大类 | |
| B. | 二氧化硫、二氧化氮是主要的大气污染物,它们能直接危害人体健康还能形成酸雨,酸雨的PH值通常小于6.5 | |
| C. | 多糖和蛋白质都是在生命活动中能起到重要作用的高分子化合物,它们的水解产物都属于烃的衍生物 | |
| D. | 合成高分子材料在现代生活中发挥着极大的作用,聚苯乙烯、酚醛树脂、涤纶、顺丁橡胶都是由单体缩聚形成的体型高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=3的CH3COOH溶液加水稀释10倍后,pH=4 | |
| B. | 25℃时,pH=11的NaOH溶液加水稀释100倍后pH=9 | |
| C. | 25℃时,pH=3的盐酸与pH=11的氨水等体积混合后,pH=7 | |
| D. | 90℃时,纯水的pH=6.2,所以加热可以使水呈酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清石灰水,浓H2SO4 | B. | 溴水,浓H2SO4 | ||
| C. | 无水硫酸铜,浓H2SO4 | D. | 浓H2SO4,酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别中和pH相同的等体积的盐酸和醋酸溶液,消耗等量的NaOH | |
| B. | pH=a的CH3COOH溶液加水稀释10n倍后,pH=a+n | |
| C. | pH相等的CH3COONa、NaOH溶液中,水的电离程度相同 | |
| D. | Na2CO3溶液中:c(OH-)=c(H+)+c(HCO${\;}_{3}^{-}$)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
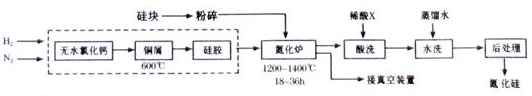
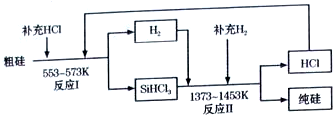
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰醋酸、纯碱、铜绿、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | Al、Al2O3、Al(OH)3均既能与盐酸反应又能与氢氧化钠反应,都属于两性化合物 | |
| D. | H2SO4、NaOH、AlCl3均为强电解质,都属于离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 运用碳及其化合物的性质,完成下列小题:
运用碳及其化合物的性质,完成下列小题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com