
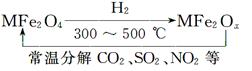
| A��MFe2O4����H2�ķ�Ӧ�б����������� |
| B��MFe2O4��MFe2Ox���ת����Ӧ������������ԭ��Ӧ |
| C��MFe2Ox��SO2��Ӧ��MFe2Ox����ԭ |
| D����4 mol MFe2Ox��1 mol SO2ǡ����ȫ��Ӧ����MFe2Ox��x��ֵΪ3��5 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 ��2FeS��SO2������ƽ���������й��ڸ÷�Ӧ��˵��������ǣ���������
��2FeS��SO2������ƽ���������й��ڸ÷�Ӧ��˵��������ǣ���������| A�������е�����ӦΪCuS |
| B���÷�Ӧ�IJ��ֲ�����������Ṥҵ |
| C����Ӧ��SO2���������������ǻ�ԭ���� |
| D����Ӧ������1 mol SO2���ɣ���һ����4 mol���ӷ���ת�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������1 mol N2������ת������Ϊ3NA | B������1 mol N2������ת������Ϊ5NA |
| C���ܽ�1 mol Zn������ת������Ϊ2NA | D���ܽ�1 mol Zn������ת������Ϊ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(NH2)2 (l) + H2O (l)��
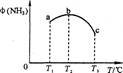
CO(NH2)2 (l) + H2O (l)�� ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ����___________��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| | 0 min | l min | 2 min | 3 min | 4 min |
| N2 | 1.500 | 1.400 | 1.200 | c1 | c1 |
| H2 | 4.500 | 4.200 | 3.600 | c2 | c2 |
| NH3 | 0 | 0.200 | 0.600 | c3 | c3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��������ǻ�ԭ�� |
| B����Ӧ������3molPʱ��ת�Ƶ��ӵ����ʵ���Ϊ15mol |
| C��KCl��������������ǻ�ԭ���� |
| D������ʱ�����İ���ֻ��KC1������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A��2F2��2H2O��4HF��O2���� | B��2Na��2H2O��2NaOH ��H2���� | C��CaO��H2O��Ca(OH)2�� | D��2H2O 2H2����O2��������(�����)�� 2H2����O2��������(�����)�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ="=" 2KCl + 2CrCl3 + 3Cl2+ 7H2O
="=" 2KCl + 2CrCl3 + 3Cl2+ 7H2O | A���٢� | B���٢ڢ� | C���٢ۢ� | D���٢� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com