
【题目】某化学小组用下列装置制取收集纯净的氯气,并研究其性质。请回答下列问题。

(1)装置甲中仪器A的名称是__,丙中应装的溶液是__,甲装置中发生反应的离子方程式为__。制取收集纯净氯气的装置接口连接顺序是a→…→g__(补充完整)。
(2)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
①方案:采用酸碱中和滴定法测定。
②进行方案实验:准确量取残余清液稀释一定倍数后作为试样。
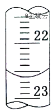
量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,对实验结果是否有影响?__(填“是”或“无”)。用0.10molL-1NaOH标准溶液滴定,消耗NaOH标准溶液的体积如右图所示,其读数为__mL。
(3)某同学认为上述方案缺少尾气吸收装置,请在下面的方框中画出该装置并注明试剂___。
【答案】分液漏斗 饱和NaCl溶液 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O debcf 无 22.60
Mn2++Cl2↑+2H2O debcf 无 22.60 
【解析】
实验设计的目的是利用装置制取、收集纯净的氯气,并研究其性质。而在制得的Cl2中,混有浓盐酸挥发出的HCl气体和水蒸气,所以应先除去HCl,再干燥去除水蒸气,最后进行氯气的性质实验;因为氯气有毒,会污染环境,所以还应有尾气处理装置。
(1)装置甲中仪器A用于添加液体,并能控制液体的用量,其名称是分液漏斗,装置丙用于除去Cl2中的HCl,所以应装入的溶液是饱和NaCl溶液,甲装置用于制取Cl2,MnO2与浓盐酸反应生成MnCl2、Cl2和H2O,发生反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。制取、收集纯净氯气时,应先除去HCl,再干燥去除水蒸气,最后进行氯气的性质实验,由此得出装置接口连接顺序是a→debcf→g。答案为:分液漏斗;饱和NaCl溶液;MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O。制取、收集纯净氯气时,应先除去HCl,再干燥去除水蒸气,最后进行氯气的性质实验,由此得出装置接口连接顺序是a→debcf→g。答案为:分液漏斗;饱和NaCl溶液;MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;debcf;
Mn2++Cl2↑+2H2O;debcf;
(2)量取试样20.00mL于锥形瓶中,若锥形瓶中存有少量水,由于样品的物质的量不变,所以对实验结果无影响。用0.10molL-1NaOH标准溶液滴定,消耗NaOH标准溶液的体积为22.60mL。答案为:无;22.60。
(3)上述方案缺少尾气吸收装置,应使用NaOH溶液吸收,且导管口插入液面下。该装置图为 。答案为:
。答案为: 。
。


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应CO(g)+H2(g)![]() C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)
C(s)+H2O(g) ΔH>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应2NO2(g)![]() N2O4(g) ΔH<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )
N2O4(g) ΔH<0的浓度(c)随时间(t)的变化情况。下列说法中正确的是( )

A. 若图一t2时改变的条件是增大压强,则反应的ΔH增大
B. 图一t2时改变的条件可能是升高了温度或增大了压强
C. 图二t1时改变的条件可能是升高了温度或增大了压强
D. 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中排放的NOx和CO污染环境,在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
Ⅰ.已知:①2CO(g)+O2(g)=2CO2(g) ΔH1=-566.0 kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180.5 kJ·mol-1
③2NO(g)+O2(g)=2NO2(g) ΔH3=-116.5 kJ·mol-1
(1)CO的燃烧热为______________。
(2)若1 mol N2(g)、1 mol O2(g)分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g)分子中化学键断裂时需吸收的能量为________。
Ⅱ.利用水煤气合成二甲醚的总反应为:
3CO(g)+3H2(g)=CH3OCH3(g)+CO2(g) ΔH=-246.4 kJ·mol-1
(3)它可以分为两步,反应分别如下:
①2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g) ΔH1=-205.1 kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2=________。
(4)已知CH3OCH3(g)的燃烧热为1455 kJ·mol-1,写出表示其燃烧热的热化学方程式:_________________________________。若二甲醚燃烧生成的CO2恰好能被100 mL 0.2 mol·L-1 NaOH溶液吸收生成Na2CO3,则燃烧过程中放出的热量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、J、Q五种短周期主族元素,原子序数依次增大。元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3:8,X能与J形成离子化合物,且J+的半径大于X-半径,Y的氧化物是形成酸雨的主要物质之一。请回答:
(1)Q元素在周期表中的位置___。
(2)将这五种元素原子半径从大到小排列,排在第三的元素原子是___(填元素符号)。
(3)元素的非金属性Z___Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有___ (填序号)
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q之间形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)若使A按下列途径完全转化为F,F的化学式为___。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别表示生物体内的生物大分子的部分结构模式图,据图回答下列问题:

(1)图甲中的三种物质的基本单位都是___________,其中属于动物细胞储能物质的是___________。这三种物质中,在功能上与另外两种截然不同的是______________________。
(2)图乙化合物是肺炎双球菌遗传物质的一部分,其基本单位是__________,可用图中字母_______表示,各基本单位之间是通过___________(填①、②或③)连接起来的。
(3)图丙所示化合物的名称是___________,是由___________种氨基酸经___________过程形成的,脱去水中的氢元素来自___________,连接氨基酸之间的化学键是___________(填化学键结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图像的解释或结论正确的是

A. 图①可表示用NaOH溶液滴定等浓度醋酸溶液,溶液导电性随NaOH的体积变化
B. 图②可表示25℃时,0.10 molL-1盐酸滴定20.00mL0.10 molL-1NaOH溶液的滴定曲线
C. 图③表示水溶液中c(H+)与c(OH-)的变化关系,则水的电离程度(![]() ):
):![]() ;水的离子积:KW(d)=KW(b)
;水的离子积:KW(d)=KW(b)
D. 图④表示合成氨N2(g)+3H2(g) ![]() 2NH3(g) △H<0的平衡常数与温度和压强的关系
2NH3(g) △H<0的平衡常数与温度和压强的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | NH3·H2O | H2CO3 | H2SO3 |
电离平衡常数 | 1.7×10-5 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.3×10-2 K2=6.3×10-8 |
请回答下列问题:
(1)H2CO3的第二级电离平衡常数的表达式K2=______。
(2)相同温度下,等pH的CH3COONa溶液、Na2CO3溶液和Na2SO3溶液,三种溶液的物质的量浓度c(CH3COONa)、c(Na2CO3)、c(Na2SO3)由大到小排序为____。
(3) 用足量Na2CO3溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为____。
(4)25℃时,向0.1 molL-1的氨水中缓缓少量CO2气体的过程中(忽略溶液体积的变化),下列表达式的数值变小的是______。
A. B.
B.
C.  D.
D.
(5)能证明醋酸是弱酸的实验事实是______(填写序号)。
① 相同条件下,浓度均为0.1 molL-1的盐酸和醋酸,醋酸的导电能力更弱
② 25℃时,一定浓度的CH3COOH、CH3COONa混合溶液的pH等于7
③ CH3COOH溶液能与NaHCO3反应生成CO2
④ 0.1molL-1 CH3COOH溶液可使紫色石蕊试液变红
(6)向冰醋酸中逐滴加水,溶液导电性随加入水的体积变化如图所示。

① a、b、c三点溶液中CH3COOH的电离程度由大到小的顺序是______。
② a、c两点对应的溶液分别吸收氨气,若两溶液最终pH均为7(25℃时),则a点溶液中的c(CH3COO-)_____c点溶液中的c(NH4+)。(填“<”、“>”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S在金属离子的鉴定分析、煤化工等领域都有着重要应用。回答下列问题:
I.工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时还生成两种能参与大气循环的氧化物。
(1)该反应的化学方程式为___。
II.H2S可用于检测和沉淀金属阳离子。
(2)由H2S制得的水溶液为氢硫酸,向氢硫酸中滴加少量的硫酸铜溶液,溶液中![]() ___(填“增大”或“减小”)。
___(填“增大”或“减小”)。
(3)已知:25℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。该温度下,向浓度均为0.1mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=___(溶液体积变化忽略不计)。
III.H2S是煤化工原料气脱硫过程的重要中间体,反应原理如下:
i.COS(g)+H2(g)![]() H2S(g)+CO(g) △H=+7kJ·mol-1;
H2S(g)+CO(g) △H=+7kJ·mol-1;
ii.CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-42kJ·mol-1。
CO2(g)+H2(g) △H=-42kJ·mol-1。
(4)已知:断裂1mol分子中的化学键所需吸收的能量如下表所示:

表中x=___。
(5)向10L溶积不变的密闭容器中充入1molCOS(g)、1molH2(g)和1molH2O(g),进行上述两个反应。
①随着温度升高,CO的平衡体积分数___(填“增大”或“减小”),其原因是___。
②T1℃时,测得平衡时体系中COS的物质的量为0.80mol,CO的体积分数为5%。则该温度下,达到平衡时H2的物质的量为___;反应i的平衡常数为___(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】直接碳固体氧化物燃料电池作为全固态的能量转换装置,采用固体碳作为燃料,以多孔Pt作电极、氧化锆为电解质,其工作原理如下图。下列说法不正确的是

已知:CO2(g)+C=2CO(g) △H=+172.5kJmol-1 CO(g)+![]() O2(g)=CO2(g)△H=-283kJmol-1
O2(g)=CO2(g)△H=-283kJmol-1
A.电极a为正极,电子由b经过导线到a
B.电极b发生的电极反应为:CO+O2--2e-=CO2
C.依据装置原理可推测,该条件下CO放电比固体C更容易
D.若1molC(s)充分燃烧,理论上放出的热量为110.5kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com