
【题目】一定温度下的恒容容器中,能标志某可逆反应2A(g)+2B(g)![]() C(g)+3D(g)己达平衡状态的是
C(g)+3D(g)己达平衡状态的是
A.混合气体的密度保持不变B.气体A的质量不随时间变化而变化
C.2v正(A)=3v逆(D)D.混合气体的压强不随时间变化而变化
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是

A. 正极反应为AgCl +e-=Ag +Cl-
B. 放电时,交换膜右侧溶液中有大量白色沉淀生成
C. 若用NaCl溶液代替盐酸,则电池总反应随之改变
D. 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】交警用三氧化铬(CrO3)硅胶可以查酒驾。元素Cr的几种化合物转化关系如图所示。下列判断正确的是
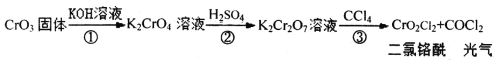
A.反应①表明CrO3有酸性氧化物的性质
B.CrO42-在碱性溶液中不能大量存在
C.只有反应③为氧化还原反应
D.基态铬原子的价电子排布式为3d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积相同的两个密闭容器M和N中,保持温度为150 ℃,向M容器中加入a mol HI,同时向N容器中加入b mol HI (a>b)。当反应2HI(g)![]() H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
A.从反应开始到达到平衡,所需时间tM > tN
B.平衡时cM(I2) = c N(I2)
C.平衡时I2 蒸气在混合气体中的体积分数:M > N
D.HI的平衡分解率αM = αN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示化学过程的化学用语书写正确的是
A.用中和热表示氢氧化钠和醋酸的稀溶液反应的热化学方程式为:H+(aq)+OH-(aq)=H2O(l) △H=57.3kJ·mol-1
B.AlCl3溶液与NaAlO2溶液混合:A13++A1O2-+3H2O![]() 2Al(OH)3↓
2Al(OH)3↓
C.HCO3-的电离:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D.Na2SO3的水解:SO32-+2H2O![]() H2SO3+2OH-
H2SO3+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molCO和3molH2O混合于2L的密闭容器中,发生如下可逆反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);
CO2(g)+H2(g);
(1)该化学反应的平衡常数表达式:___。
(2)已知在700℃时,该反应的平衡常数K1=2,则该温度下反应CO2(g)+H2(g)CO(g)+H2O(g)的平衡常数K2=__,反应2CO(g)+2H2O(g)2CO2(g)+2H2(g)的平衡常数K3=___。
(3)已知在1000℃时,该反应的平衡常数K4=1.0,则该反应为___反应(填“吸热”或“放热”),△H__0(填“>”或“<”)。
(4)在1000℃下,某时刻CO2的物质的量为1mol,则此时υ(正)__υ(逆)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是草本植物常具有的成分。查阅相关资料得到草酸晶体(H2C2O4·3H2O)及其盐的性质如下表。

(1)草酸晶体(H2C2O4·3H2O)175℃以上会发生分解生成三种氧化物,某实验小组欲通过实验证明这三种氧化物。
①该小组选用装置丙作为分解装置,不选用甲装置的原因是________________。丙装置相对于乙装置的优点是____________。实验前检验该装置气密性的操作方法是_________。

②从下图选用合适的装置,验证分解产生的气体,装置的连接顺序是____________。(用装置编号表示,某些装置可以重复使用,也可以装不同的试剂)

③B装置的作用是________________________。
(2)某实验小组称取4.0g粗草酸晶体配成100mL溶液,采用0.1mol·L-1酸性高锰酸钾溶液滴定该草酸溶液,测定该草酸晶体的纯度。
①配制草酸溶液需要用到的主要玻璃仪器有_______________。
②本实验达到滴定终点的标志是______________________。
③将所配草酸分为四等份,实验测得每份平均消耗酸性高锰酸钾溶液20mL。计算该粗草酸中含草酸晶体的质量为_______g(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液滴加到HA溶液中,测得混合溶液的pH与p![]() 转化关系如图所示[已知:p
转化关系如图所示[已知:p![]() =-lg
=-lg![]() ]。下列叙述错误的是( )
]。下列叙述错误的是( )
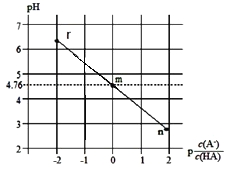
A.m点:c(A-)=c(HA)
B.Ka(HA)的数量级为10-6
C.水的电离程度:m<r
D.r点:c(H+)+c(Na+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4 ①
R-OH+HBr![]() R-Br+H2O ②
R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等。有关数据列表如下:
乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答:
(1)得到的溴乙烷中含有少量乙醇,为了制得纯净的溴乙烷,可用蒸馏水洗涤,分液后,再加入无水CaCl2,然后进行的实验操作是___(填字母)。
a.分液 b.蒸馏 c.萃取 d.过滤
(2)溴乙烷的水溶性___乙醇(填“大于”、“等于”或“小于”),其原因是___。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在___(填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必须进行稀释,其目的是___(填字母)。
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)为了检验溴乙烷中含有溴元素,通常采用的方法是:取少量溴乙烷,然后进行下列操作:①加热 ②加入AgNO3溶液 ③加入稀HNO3酸化 ④加入NaOH溶液。下列操作顺序合理的是___(填字母)。
a.①②③④ b.②③①④ c.④①③② d. ①④②③
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com