
 丙烯酰胺是一种重要的有机合成的中间体.它的球棍模型如图所示:(图中“棍”代表单键或双键或三健,不同颜色球表示不同原子:C、H、O、N)
丙烯酰胺是一种重要的有机合成的中间体.它的球棍模型如图所示:(图中“棍”代表单键或双键或三健,不同颜色球表示不同原子:C、H、O、N) .
. 分析 (1)由图可知,绿球代表C、白球代表H、红球为O、蓝球为N,以此分析;
(2)含C=C及-CO-NH-,利用烯烃及酰胺键来分析;
(3)由合成可知,Ⅰ发生与HCN的加成,Ⅱ为与水的反应.
解答 解:(1)由图可知,绿球代表C、白球代表H、红球为O、蓝球为N,则分子式为C3H5ON,结构简式为CH2=CHCONH2,
故答案为:CH2=CHCONH2;
(2)含C=C及-CO-NH-,则
A.丙烯酰胺分子内中存在氨基,则所有原子不可能在同一平面内,故A正确;
B.丙烯酰胺中含C、H、N、O四种元素,则不属于烃的含氧衍生物,故B错误;
C.丙烯酰胺中含C=C,则能够使酸性高锰酸钾溶液褪色,故C正确;
D.丙烯酰胺中含C=C,则能够使溴的四氯化碳溶液褪色,故D错误;
故答案为:AC;
(3)由合成可知,Ⅰ乙炔发生与HCN的加成,Ⅱ为与水的加成反应,该反应为 ,
,
故答案为:HCN; .
.
点评 本题考查有机物的结构与性质,注意有机物的官能团与性质的关系,熟悉加成反应及加聚反应即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. |  | B. | CH3-CH2-CH2-CH2-OH | ||
| C. | CH2=CHCl | D. | 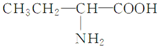 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14C与14N含有相同的中子数 | |
| B. | 14C与C60是同分异构体 | |
| C. | 14C与C60中普通碳原子的化学性质不同 | |
| D. | 14C与12C互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 稀NH4Cl溶液和稀NaOH溶液作用:NH4++OH-═NH3↑+H2O | |
| C. | 氨气通入醋酸溶液中:CH3COOH+NH3═CH3COONH4 | |
| D. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 HClO+OH-
HClO+OH-查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | baedc | B. | edabc | C. | abdce | D. | ebadc |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com