
ЁОЬтФПЁПЬхг§ОКММжаЗўгУаЫЗмМСМШгаЪЇЙЋЦНЃЌвВАмЛЕСЫЬхг§ЕРЕТЁЃФГжжаЫЗмМСЕФНсЙЙМђЪНШчЭМЫљЪОЁЃгаЙиИУЮяжЪЕФЫЕЗЈжае§ШЗЕФЪЧ(ЁЁЁЁ)
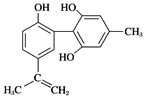
A. ИУЮяжЪгіFeCl3ШмвКГЪзЯЩЋЃЌЧвЪєгкБНЗгЭЌЯЕЮя
B. ЕЮШыЫсадKMnO4ШмвКеёЕДЃЌзЯЩЋЭЪШЅЃЌФмжЄУїЦфНсЙЙжаДцдкЬМЬМЫЋМќ
C. 1 molИУЮяжЪЗжБ№гыХЈфхЫЎКЭH2ЗДгІЪБзюЖрЯћКФBr2КЭH2ЗжБ№ЮЊ4 molКЭ7 mol
D. ИУЗжзгжаЫљгаЬМдзгвЛЖЈЙВЦНУц
ЁОД№АИЁПC
ЁОНтЮіЁП
AЃЎБНЗгЭЌЯЕЮяжажЛКЌ1ИіБНЛЗЃЌИУЮяжЪКЌ2ИіБНЛЗЃЌВЛЪЧБНЗгЭЌЯЕЮяЃЌЕЋКЌЗг-OHЃЌгіFeCl3ШмвКГЪзЯЩЋЃЌбЁЯюAДэЮѓЃЛBЃЎЬМЬМЫЋМќЁЂЬМЬМШ§МќЁЂЗг-OHЁЂДМ-OHЕШОљФмБЛбѕЛЏЃЌЕЮШыЫсадKMnO4ШмвКеёЕДЃЌзЯЩЋЭЪШЅЃЌВЛФмФмжЄУїЦфНсЙЙжаЬМЬМЫЋМќЁЂЗгєЧЛљСНжжЛљЭХжСЩйДцдквЛжжЃЌбЁЯюBДэЮѓЃЛCЃЎЗг-OHЕФСкЖдЮЛгыфхЫЎЗЂЩњШЁДњЃЌЬМЬМЫЋМќгыфхЫЎЗЂЩњМгГЩЃЌдђ1molИУЮяжЪгыХЈфхЫЎЗДгІЃЌЯћКФфхЮЊ4molЃЛБНЛЗгыЬМЬМЫЋМќОљгыЧтЦјЗЂЩњМгГЩЃЌдђ1molИУЮяжЪгыЧтЦјЗДгІЪБЃЌЯћКФЧтЦјЮЊ7molЃЌбЁЯюCе§ШЗЃЛDЃЎБНЛЗЁЂЬМЬМЫЋМќОљЮЊЦНУцНсЙЙЃЌЧвжБНгЯрСЌЕФдзгдкЭЌвЛЦНУцФкЃЌдђИУЗжзгжаЕФЫљгаЬМдзгПЩФмЙВЦНУцЃЌбЁЯюDДэЮѓЃЛД№АИбЁCЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇбЇЯАаЁзщНјааШчЯТЪЕбщВтЖЈ H2C2O4ЁЄxH2O жа x жЕвбжЊЃКMЃЈH2C2O4ЃЉ=90gmol-1
Ђй ГЦШЁ1.260 g ДПВнЫсОЇЬхЃЌНЋВнЫсжЦГЩ 100.00 mL ЫЎШмвКЮЊД§ВтвКЃЛ
Ђк ШЁ25.00 mL Д§ВтвКЗХШызЖаЮЦПжаЃЌдйМгШыЪЪСПЕФЯЁ H2SO4ЃЛ
Ђл гУХЈЖШЮЊ 0.05 000 molЁЄL-1 ЕФ KMnO4БъзМШмвКНјааЕЮЖЈЁЃ
(1)ЧыаДГіЕЮЖЈжаЗЂЩњЗДгІЕФРызгЗНГЬЪН________________________ЁЃ
(2)ФГбЇЩњЕФЕЮЖЈЗНЪНЃЈМаГжВПЗжТдШЅЃЉШчЯТЃЌзюКЯРэЕФЪЧ_____ЃЈбЁЬю aЁЂbЃЉЁЃ
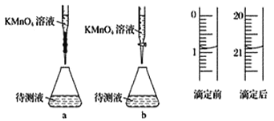
(3)гЩЭМПЩжЊЯћКФ KMnO4 ШмвКЬхЛ§ЮЊ________mLЁЃ
(4)ЕЮЖЈЙ§ГЬжаблОІгІзЂЪг_______________ЃЌЕЮЖЈжеЕузЖаЮЦПФкШмвКЕФбеЩЋБфЛЏЮЊ_______ЁЃ
(5)ЭЈЙ§ЩЯЪіЪ§ОнЃЌЧѓЕУ x=_____ЁЃ
a.ШєгЩгкВйзїВЛЕБЃЌЕЮЖЈНсЪјКѓЕЮЖЈЙмМтзьДІгавЛЦјХнЃЌ в§Ц№ЪЕбщНсЙћ_____ЃЈЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЃЛ
b.ШєдкНгНќжеЕуЪБЃЌгУЩйСПеєСѓЫЎНЋзЖаЮЦПГхЯДвЛЯТЃЌдйМЬајЕЮЖЈжСжеЕуЃЌдђЫљВтНсЙћ_______(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБ)ЃЛ
c.ШєдкДяЕНЕЮЖЈжеЕуЪБбіЪгЖСЪ§ЃЌдђЫљЕУНсЙћ________(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБ)ЃЛ
d.ШєЦфЫќВйзїОље§ШЗЃЌЕЮЖЈЧАЮДгУБъзМ KMnO4 ШмвКШѓЯДЕЮЖЈЙмЃЌв§Ц№ЪЕбщНсЙћ_________ЃЈЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкУмБеШнЦїжаЭЈШывЛЖЈСПЕФHIЦјЬхЃЌЪЙЦфдквЛЖЈЬѕМўЯТЗЂЩњЗДгІЃК2HI(g)![]() H2(g)ЃЋI2(g)ЁЃЯТСаа№ЪіжаЃЌвЛЖЈЪєгкЦНКтзДЬЌЕФЪЧ
H2(g)ЃЋI2(g)ЁЃЯТСаа№ЪіжаЃЌвЛЖЈЪєгкЦНКтзДЬЌЕФЪЧ
A. HIЁЂH2ЁЂI2ЕФХЈЖШЯрЕШ
B. ЛьКЯЦјЬхЕФбеЩЋВЛдйБфЛЏ
C. ЛьКЯЦјЬхЕФзмбЙЧПВЛдйБфЛЏ
D. v(HI)ЁУv(H2)ЁУv(I2)ЃН2ЁУ1ЁУ1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂWЫФжжЖЬжмЦкжїзхдЊЫиЕФдзгађЪ§вРДЮдіДѓЁЃXЁЂYдзгЕФзюЭтВуЕчзгЪ§жЎБШЮЊ2ЁУ3ЃЌZ+гыY2-КЫЭтЕчзгХХВМЭъШЋЯрЭЌЃЌГЃЮТЯТ,WЕФвЛжжЕЅжЪЮЊЕЛЦЩЋЙЬЬхЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
A. РызгАыОЖЃКW>Z>Y
B. МђЕЅЦјЬЌЧтЛЏЮяЕФШШЮШЖЈадЃКY>W
C. YЗжБ№гыXЁЂZЁЂWФмаЮГЩСНжжЛђСНжжвдЩЯЕФЛЏКЯЮя
D. ZгыYЁЂWЗжБ№аЮГЩЕФЛЏКЯЮяШмгкЫЎЃЌШмвКОљГЪМюад
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПАБЪЧЛЏбЇЪЕбщЪвМАЛЏЙЄЩњВњжаЕФживЊЮяжЪЃЌгІгУЙуЗКЁЃ
ЃЈ1ЃЉвбжЊ25ЁцЪБЃКN2(g)ЃЋO2(g)![]() 2NO(g) ІЄH=+183 kJ/mol
2NO(g) ІЄH=+183 kJ/mol
2H2(g)ЃЋO2(g)ЃН2H2O(l) ІЄH=Ѓ571.6 kJ/mol
4NH3(g)ЃЋ5O2(g)ЃН4NO(g)ЃЋ6H2O(l) ІЄH=Ѓ1164.4 kJ/mol
дђN2(g)ЃЋ3H2(g)![]() 2NH3(g) ІЄH=______kJ/mol
2NH3(g) ІЄH=______kJ/mol
ЃЈ2ЃЉдкКуЮТКуШнУмБеШнЦїжаНјааКЯГЩАБЗДгІЃЌЦ№ЪМЭЖСЯЪБИїЮяжЪХЈЖШШчЯТБэЃК
N2 | H2 | NH3 | |
ЭЖСЯЂё | 1.0 mol/L | 3.0 mol /L | 0 |
ЭЖСЯЂђ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
ЂйАДЭЖСЯЂёНјааЗДгІЃЌВтЕУДяЕНЛЏбЇЦНКтзДЬЌЪБH2ЕФзЊЛЏТЪЮЊ40%ЃЌдђИУЮТЖШЯТКЯГЩАБЗДгІЕФЦНКтГЃЪ§БэДяЪНЮЊ_______ЁЃ
ЂкАДЭЖСЯЂђНјааЗДгІЃЌЦ№ЪМЪБЗДгІНјааЕФЗНЯђЮЊ________ЃЈЬюЁАе§ЯђЁБЛђЁАФцЯђЁБЃЉЁЃ
ЂлШєЩ§ИпЮТЖШЃЌдђКЯГЩАБЗДгІЕФЛЏбЇЦНКтГЃЪ§________ЃЈЬюЁАБфДѓЁБЁЂЁАБфаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЂмLЃЈL1ЁЂL2ЃЉЁЂXПЩЗжБ№ДњБэбЙЧПЛђЮТЖШЁЃЯТЭМБэЪОLвЛЖЈЪБЃЌКЯГЩАБЗДгІжаH2(g)ЕФЦНКтзЊЛЏТЪЫцXЕФБфЛЏЙиЯЕЁЃ

ЂЁ XДњБэЕФЮяРэСПЪЧ______ЁЃ
ЂЂ ХаЖЯL1ЁЂL2ЕФДѓаЁЙиЯЕЃЌВЂМђЪіРэгЩ______ЁЃ
ЃЈ3ЃЉЕчЛЏбЇЦјУєДЋИаЦїПЩгУгкМрВтЛЗОГжаNH3ЕФКЌСПЃЌЦфЙЄзїдРэЪОвтЭМШчЯТЃК
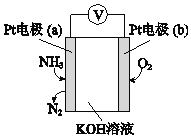
ЂйЕчМЋbЩЯЗЂЩњЕФЪЧ______ЗДгІЃЈЬюЁАбѕЛЏЁБЛђЁАЛЙдЁБЃЉЁЃ
ЂкаДГіЕчМЋaЕФЕчМЋЗДгІЪН_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЁЂBЕФНсЙЙМђЪНШчЯТЃК

(1)AЗжзгжаКЌгаЕФЙйФмЭХЕФУћГЦЪЧ____________________________________ЁЃ
(2)AЁЂBФмЗёгыNaOHШмвКЗДгІЃКA________(ЬюЁАФмЁБЛђЁАВЛФмЁБЃЌЯТЭЌ)ЃЌB________ЁЃ
(3)AдкХЈСђЫсзїгУЯТМгШШПЩЕУЕНBЃЌЦфЗДгІРраЭЪЧ____________________ЁЃ
(4)AЁЂBИї1 molЗжБ№МгШызуСПфхЫЎЃЌЭъШЋЗДгІКѓЯћКФЕЅжЪфхЕФЮяжЪЕФСПЗжБ№ЪЧ________molЁЂ________molЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГгаЛњЮяМгЧтЗДгІКѓЩњГЩ ![]() ЃЌИУгаЛњЮяПЩФмЪЧ
ЃЌИУгаЛњЮяПЩФмЪЧ
A. ввШЉЕФЭЌЯЕЮя B. ЮьШЉЕФЭЌЗжвьЙЙЬх
C. БћДМЕФЭЌЯЕЮя D. ЖЁДМЕФЭЌЗжвьЙЙЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЁЂWЪЧЗжБ№ЮЛгкЕк2ЁЂ3жмЦкЕФдЊЫиЃЌдзгађЪ§вРДЮЕндіЁЃXгыZЮЛгкЭЌвЛжїзхЃЌYдЊЫиЕФЕЅжЪМШФмгыбЮЫсЗДгІвВФмгыNaOHШмвКЗДгІЃЌZдзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФвЛАыЃЌYЁЂZЁЂWдзгЕФзюЭтВуЕчзгЪ§жЎКЭЮЊ14ЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ)
A. дзгАыОЖгЩаЁЕНДѓЕФЫГађЃКX< Y < Z< W
B. ZЕФзюИпМлбѕЛЏЮяФмгыЫЎЗДгІЩњГЩЯргІЕФЫс
C. YЕЅжЪдквЛЖЈЬѕМўЯТПЩвдгыбѕЛЏЬњЗЂЩњжУЛЛЗДгІ
D. XЁЂZЕФбѕЛЏЮяаЮГЩЕФОЇЬхРраЭЯрЭЌ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌЫЎДцдкH2O![]() H++OH--QЕФЦНКтЃЌЯТСаа№ЪівЛЖЈе§ШЗЕФЪЧ
H++OH--QЕФЦНКтЃЌЯТСаа№ЪівЛЖЈе§ШЗЕФЪЧ
A. ЯђЫЎжаЕЮШыЩйСПЯЁбЮЫсЃЌЦНКтФцЯђвЦЖЏЃЌKwМѕаЁ
B. НЋЫЎМгШШЃЌKwдіДѓЃЌpHМѕаЁ
C. ЯђЫЎжаМгШыЩйСПЙЬЬхCH3COONaЃЌЦНКтФцЯђвЦЖЏЃЌc(H+)НЕЕЭ
D. ЯђЫЎжаМгШыЩйСПЙЬЬхNH4ClЃЌc(H+)=10-7mol/LЃЌKwВЛБф
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com