
【题目】某化学学习小组进行如下实验测定 H2C2O4·xH2O 中 x 值已知:M(H2C2O4)=90gmol-1
① 称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液;
② 取25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4;
③ 用浓度为 0.05 000 mol·L-1 的 KMnO4标准溶液进行滴定。
(1)请写出滴定中发生反应的离子方程式________________________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是_____(选填 a、b)。
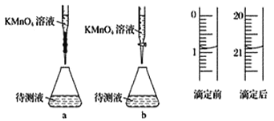
(3)由图可知消耗 KMnO4 溶液体积为________mL。
(4)滴定过程中眼睛应注视_______________,滴定终点锥形瓶内溶液的颜色变化为_______。
(5)通过上述数据,求得 x=_____。
a.若由于操作不当,滴定结束后滴定管尖嘴处有一气泡, 引起实验结果_____(填“偏大”、“偏小”或“无影响”);
b.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果_______(填“偏大”、“偏小”或“无影响”);
c.若在达到滴定终点时仰视读数,则所得结果________(填“偏大”、“偏小”或“无影响”);
d.若其它操作均正确,滴定前未用标准 KMnO4 溶液润洗滴定管,引起实验结果_________(填“偏大”、“偏小”或“无影响”)。
【答案】5H2C2O4+2MnO4- +6H+ ===10CO2 ↑+2Mn2+ +8H2O b 20.00 锥形瓶中颜色变化 溶液由无色变成紫红色,且半分钟内不褪色 2 偏小 无影响 偏大 偏大
【解析】
(1)H2C2O4溶液和酸性KMnO4溶液反应生成二氧化碳、锰离子和水;
(2)据高锰酸钾呈酸性,盛放在酸式滴定管中来选择;
(3)根据滴定管的结构、精确度以及测量原理来解答;
(4)据滴定终点的判断是溶液中颜色的变化来分析;
(5)据此6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O离子方程式来计算;据滴定过程中眼睛应注视溶液中颜色变化,来判断滴定终点分析;根据 c(待测)=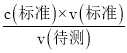 分析不当操作对V(标准)的影响,以此判断浓度的误差。
分析不当操作对V(标准)的影响,以此判断浓度的误差。
(1)H2C2O4溶液和酸性KMnO4溶液反应生成二氧化碳、锰离子和水,其反应的离子方程式为:6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O;
(2)高锰酸钾溶液呈酸性,应盛放在酸式滴定管中,故答案为b;
(3)该仪器是酸式滴定管,滴定管滴定前后读数为:0.80mL,20.80mL,消耗KMnO4溶液体积为20.80mL-0.80mL=20.00mL;
(4)据酸性KMnO4溶液为紫红色,滴定终点时无色变为紫红色,且半分钟不褪色为滴定到终点故眼睛应注视溶液中颜色变化;
(5)6H++5H2C2O4+2MnO4-=2Mn2++10CO2↑+8H2O
5 2
n=0.00250.02×0.05
m(H2C2O4)=0.0025×90=0.225g;m(H2C2O4xH2O )=1.26×![]() =0.315g;
=0.315g;
m(H2O)=0.315-0.225=0.09g;n(H2O)=![]() mol=0.005mol①
mol=0.005mol①
又因为 n H2C2O4)=0.0025 mol根据元素守恒即n(H2C2O4xH2O )=0.0025mol;n(H2O)=0.0025x②;联立①②得0.005=0.0025x,解得x=2;
a. 滴定结束后滴定管尖嘴处有一气泡,消耗标准液的体积偏小,根据 c(待测)=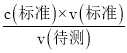 ,导致测定结果偏小;
,导致测定结果偏小;
b.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,不影响消耗标准溶液的体积,根据 c(待测)=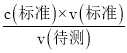 ,则测定结果无影响;
,则测定结果无影响;
c.若在达到滴定终点时仰视读数,造成V(标准)偏大,根据 c(待测)=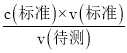 故c(待测)偏大;
故c(待测)偏大;
d.未用标准KMnO4溶液润洗滴定管,溶液被稀释,造成V(标准)偏大,根据 c(待测)=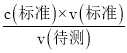 故c(待测)偏大;
故c(待测)偏大;


科目:高中化学 来源: 题型:
【题目】(1)基态溴原子的价层电子轨道排布式为________。第四周期中,与溴原子未成对电子数相同的金属元素有_______种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________(填标号)。
A.都属于p区主族元素B.电负性都比镁大
C.第一电离能都比镁大D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________;[AlCl4]-的立体构型名称为______。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________。

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 丙烯分子中所有原子均在同一平面上
B. ![]() 命名为2-甲基-3-丁炔
命名为2-甲基-3-丁炔
C. 化合物![]() 不是苯的同系物
不是苯的同系物
D. C5H12的同分异构体数目与甲苯的一氯代物数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种短周期主族元素z、e、g、h,其最高价氧化物对应水化物溶液(浓度均为0.01molL﹣1)的pH与原子序数的关系如图所示。下列说法正确的是

A. 离子半径大小 e>g>h
B. g位于第三周期VA族
C. e2g2中即含有离子键有含有非极性共价键
D. 同浓度简单氢化物水溶液的pH值 h >g> z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Fe2+、Fe3+和FeO42-的性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液。在FeCl2溶液中需加入少量铁屑,其目的是________;将FeCl3晶体溶于浓盐酸,再稀释到需要的浓度,盐酸的作用是________。
(2)制备K2FeO4(夹持装置略)后,取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
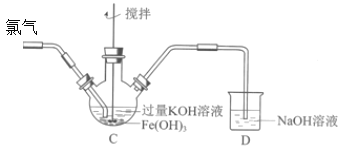
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________。根据K2FeO4的制备原理3Cl2+2Fe(OH)3+10KOH=2K2FeO4+6KCl+8H2O得出:氧化性Cl2______FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示(明矾石焙烧后成分不变):
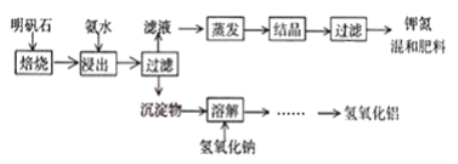
完成下列填空:
(1)“浸出”反应的离子方程式为_______。“浸出”所用稀氨水浓度为39.20g/L,配制500mL该氨水需251.28g/L的浓氨水________mL。
(2)“过滤”所需的玻璃仪器有______________。
(3)写出“溶解”过程中发生反应的化学方程式_________、________。
(4)检验滤液中是否含有SO42-的实验方法__________。
(5)为测定钾氨复合肥K2SO4、(NH4)2SO4中SO42-的质量分数,设计实验步骤如下:
①_____________________。
②溶于水,加入足量BaCl2溶液,待白色沉淀不再产生为止。
③过滤、______、________(依次填写实验操作名称)。
④冷却、称量所得沉淀的质量。
(6)若所取试样和所得沉淀的质量分别为mg、ng,试用含有m、n的代数式表示该钾氮复合肥中SO42-的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图:
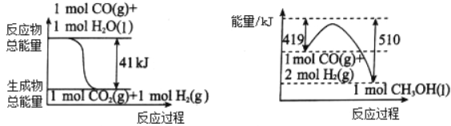
则CO2与H2反应生成CH3OH的热化学方程式为_____________________
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH;
I.CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1>0
CO(g)+3H2(g) △H1>0
Ⅱ.CO(g)+2H2(g)![]() CH3OH(g) △H2<0
CH3OH(g) △H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如下图所示。
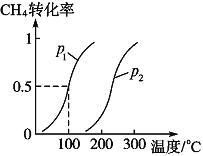
①已知温度为T1℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为________;
②图中的p1_______p2(填“<”、“>”或“=”),判断的理由是________________________。
③若反应Ⅱ在恒容密闭容器进行,下列能判断反应Ⅱ达到平衡状态的是_________(填序号)。
a.生成CH3OH的速率与消耗CO的速率相等
b.混合气体的密度不变
c.混合气体的总物质的量不变
d.CH3OH、CO、H2的浓度都不再发生变化
④在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol·L﹣1)变化如下表所示:
2min | 5min | 10min | |
CO | 0.07 | 0.06 | 0.05 |
H2 | 0.14 | 0.12 | 0.20 |
CH3OH | 0.03 | 0.04 | 0.05 |
若5min时只改变了某一条件,则所改变的条件是_____________;10min时测得各物质浓度如表,10min时v正_______v逆(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体育竞技中服用兴奋剂既有失公平,也败坏了体育道德。某种兴奋剂的结构简式如图所示。有关该物质的说法中正确的是( )
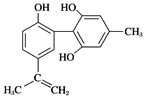
A. 该物质遇FeCl3溶液呈紫色,且属于苯酚同系物
B. 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
C. 1 mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2分别为4 mol和7 mol
D. 该分子中所有碳原子一定共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com