
【题目】有四种短周期主族元素z、e、g、h,其最高价氧化物对应水化物溶液(浓度均为0.01molL﹣1)的pH与原子序数的关系如图所示。下列说法正确的是

A. 离子半径大小 e>g>h
B. g位于第三周期VA族
C. e2g2中即含有离子键有含有非极性共价键
D. 同浓度简单氢化物水溶液的pH值 h >g> z
【答案】C
【解析】由图象可知,四种元素最高价氧化物对应的水化物溶液的浓度为0.01mol/L,其中z对应pH为2,即为强酸,结合原子序数可知z为N元素,e对应的pH为12,即为强碱,所以e为Na元素,所以推出g为S元素,h为Cl元素。所以Na、S、Cl的离子半径大小为S2->Cl->Na+,即g>h>e,所以A错误;S元素位于第三周期ⅥA族,则B错误;C、e2g2即Na2S2,类似于Na2O2,所以分子内既含有离子键,又含有非极性共价键,所以C正确;D、h、g、z三种元素的简单氢化物分别为HCl、H2S、NH3,同浓度时三者水溶液的pH大小关系为NH3> H2S> HCl,即z >g >h,所以D错误。本题正确答案为C。


科目:高中化学 来源: 题型:
【题目】化学是一门实用性的学科,以下叙述正确的是( )
A. 静置后的淘米水能产生丁达尔现象,这种“淘米水”是胶体
B. “洁厕灵”有效成分为盐酸,与漂白粉混合使用效果更佳
C. 活泼金属的冶炼常用电解方法,如电解NaCl溶液就可制备Na
D. 铝热反应中可得到铁,工业上可以利用该反应来大量生产铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A既能使溴水褪色,又能与碳酸钠溶液反应放出CO2 . A与CnH2n+1OH反应生成分子式为Cn+3H2n+4O2的酯,回答以下问题:
(1)A的分子式为: , 结构简式为: .
(2)已知含碳碳双键的有机物与卤化氢发生加成反应时,氢原子总是加到含氢较多的双键碳原子上.依此规则,A与HBr发生加成反应生成的物质B的结构简式为: .
(3)B与足量NaOH溶液发生反应生成C的化学方程式是: .
(4)C处理后,一定条件下生成的聚合物的结构简式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牛通过吃草从草中获得化合物和元素,那么,牛和草体内的各种化学元素( )
A.种类差异很大,含量大体相同
B.种类和含量差异都很大
C.种类和含量都是大体相同的
D.种类大体相同,含量差异很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体[Cu(NH3)4]SO4·H2O。
(1)Cu2+基态核外电子排布式为________________________;[Cu(NH3)4]SO4·H2O中,不考虑空间构型,[Cu(NH3)4]2+的结构可用示意图表示为___________。
(2)乙醇分子中C原子轨道杂化类型为___________,H2O与H+以配位键形成H3O+,则H3O+的空间构型为__________(用文字描述)。
(3)N、O、S第一电离能由大到小的顺序为____________________。
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是________。
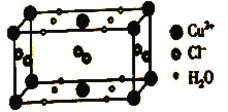
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。下列说法错误的是

A. ②的作用是安全瓶
B. ③中试剂更换为Ba(NO3)2后,无明显现象发生
C. ④中的现象说明SO2具有氧化性
D. ⑤用于检验SO2的漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电动汽车以锂电池提供动力,锂电池技术已经成为汽车研究的前沿科技某锂电池的电池反应为:xLi+Li3-xNiCoMnO6![]() Li3NiCoMnO6,下列说法正确的是
Li3NiCoMnO6,下列说法正确的是![]()
A. 该电池的充、放电过程互为可逆反应
B. 放电时,电池的负极反应为Li-e-=Li+
C. 放电过程中,Li+向电池的负极移动
D. 该电池可以采用醋酸、乙醇等作为电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、U、W 是原子序数依次增大的前四周期元素。其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子。请回答下列问题:
(1)U 在周期表中的位置 。X、Y、Z 的第一电离能从大到小的顺序是 (用元素符号表示,下同)。
(2)写出 W 的价电子排布图 。
(3)根据等电子体原理,可知化合物 XZ 的电子式是 。
(4)X、Y、Z的最简单氢化物的键角从大到小的顺序是 ( 用化学式表示), 原因 是 。
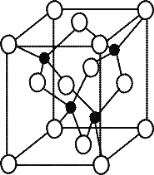
(5)由元素 Y 与 U 元素组成的化合物 A,晶胞结构如右图所示(黑球表示 Y 原子, 白球表示 U 原子),请写出化合物 A 的化学式 ,其中 Y 元素的杂化方式是 。
(6)U 的晶体属立方晶系,其晶胞边长为 405 pm,密度是 2.70 g/cm,通过计算确定 其晶胞的类型 (填简单立方堆积、体心立方堆积或面心立方最密堆 积)(已知:4053≈6.64×107)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在恒容密闭容器中发生反应2HI(g)+Cl2(g)![]() 2HCl(g) +I2(s)。下列事实不能说明该反应达到平衡状态的是
2HCl(g) +I2(s)。下列事实不能说明该反应达到平衡状态的是
A. 断裂1mol Cl-Cl键的同时形成2molH-Cl键
B. 容器内气体密度不再改变
C. 容器内气体颜色不再改变
D. 容器内气体压强不再改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com