
在日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等名词,这里的碘、铁、钙、硒、氟应理解为
A.单质 B.元素 C.分子 D.氧化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
有以下几种物质:①食盐晶体 ②乙醇 ③水银 ④蔗糖 ⑤冰醋酸(纯醋酸晶体)⑥KNO3溶液 ⑦熔融的氢氧化钠 ⑧液态氯化氢 填空回答(填序号):
(1)以上物质可以导电的是 ;
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的离子方程式书写正确的是
A.氯气通入氯化亚铁溶液中:Fe2++Cl2== 2Cl-+Fe3+
B.氯气与水反应:Cl2 + H2O== Cl-+ ClO- + 2H+
C.铜与稀硝酸反应:3Cu + 8H+ + 2NO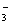 == 3Cu2+ + 2NO↑ + 4H2O
== 3Cu2+ + 2NO↑ + 4H2O
D.三氯化铝中加入过量的氨水:Al3++4 NH3·H2O = AlO2— +4 NH4+ + 2 H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 2 | 1 | 2 | 3 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
在1L密闭容器中通入10 molCO和10 mol水蒸气,在500℃下经过30s达
到平衡,则30s内CO的平均反应速率为
(3)已知在一定温度下,C(s)+CO2(g)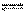 2CO(g)平衡常数K;K的表达式 ;
2CO(g)平衡常数K;K的表达式 ;
C(s)+H2O(g)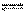 CO(g)+ H2(g)平衡常数K1;
CO(g)+ H2(g)平衡常数K1;
CO(g)+H2O(g)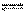 H2(g)+ CO2(g)平衡常数K2;
H2(g)+ CO2(g)平衡常数K2;
则K、K1、K2之间的关系是:
某温度、容积固定容器中,投入一定反应物,对可逆反应
C(s)+ CO2(g)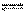 2CO(g)不能判断该反应达到化学平衡状态的是
2CO(g)不能判断该反应达到化学平衡状态的是
A.c(CO2)= c(CO) B.混合气体相对分子质量不变
C.容器中的压强不变 D.v正(CO)= 2v正(CO2) E.c(CO)保持不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙
两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g) 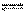 2CO(g),
2CO(g),
并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的
图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.

查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.纤维素属于多糖,在人体内水解转化为葡萄糖,也可为人类提供能量
B.糖尿病患者吃糖量必须限制,但淀粉类食物不必进行限制
C.同质量的脂肪在体内氧化放出的能量比糖类和蛋白质高得多,是提供能量的主要物质
D.葡萄糖在人体内不可以转化为脂肪,所以吃糖不会使人发胖
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室中,对下列事故或药品的处理正确的是
A . 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场
B. 金属钠着火燃烧时,用泡沫灭火器灭火
C. 少量浓硫酸沾在皮肤上,立即用大量的氢氧化钠溶液冲洗
D. 含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
如图判断,下列说法正确的是 ]
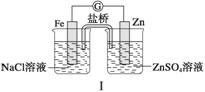
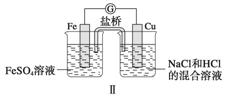
A.装置Ⅰ和装置Ⅱ中负极反应均是Fe-2e-===Fe2+
B.装置Ⅰ和装置Ⅱ中正极反应均是O2+2H2O+4e-===4OH-
C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的pH均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下。
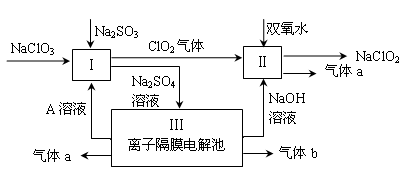 |
(1)Ⅰ中发生反应的还原剂是 (填化学式)。
(2)Ⅱ中反应的离子方程式是 。
(3)A的化学式是 ,气体b的化学式是 ,
装置Ⅲ中发生反应的化学方程式是 。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
5NaClO2 + 4HCl = 5NaCl + 4ClO2↑ + 2H2O。
① 该反应中氧化剂和还原剂的物质的量之比是 。
② 研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com