
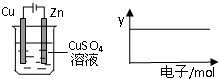
 按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )| A、c(Cu2+) |
| B、c(SO42-) |
| C、Cu棒的质量 |
| D、溶液的pH |


科目:高中化学 来源: 题型:
| A、Zn+2HCl═ZnCl2+H2↑ | ||||
| B、BaCl2+H2SO4═BaSO4↓+2HCl | ||||
C、H2+CuO
| ||||
| D、Fe+CuSO4═FeSO4+Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4═H++SO42- |
| B、Al2(SO4)3=2Al3++3SO42- |
| C、KClO3=K++3O2-+Cl5+ |
| D、NaHSO4=Na++HSO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都是常用的干燥剂 |
| B、一定条件下都能与铜等金属反应 |
| C、常温下都可以储存于铝制槽罐中 |
| D、敞口露置于空气中,一段时间后,容器内的溶质的物质的量浓度都降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子化合物可能含共价键,共价化合物中不含离子键 |
| B、共价化合物可能含离子键,离子化合物中只含离子键 |
| C、阴阳离子间通过静电吸引形成的化学键叫离子键 |
| D、由非金属元素组成的化合物都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com