
A��5NH4NO3
| ||||
| B�������£�1 L pH=13��NaOH��Һ�У���ˮ�����OH-��ĿΪ0.1NA | ||||
| C������ȼ�ϵ����������22.4 L����״��������ʱ����·��ͨ���ĵ�����ĿΪ2NA | ||||
| D�������£�0.2 mol Fe������ˮ������Ӧ�����ɵ�H2������ĿΪ0.3 NA |
| 8 |
| 3 |
| 15 |
| 4 |
| 8 |
| 3 |
| 1.6mol |
| 3 |
| 1.6mol |
| 3 |
| 1 |
| 2 |
| 4 |
| 15 |
| 4 |
| 15 |


 ������ÿ�ʱ�Ż���ҵϵ�д�
������ÿ�ʱ�Ż���ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��Ca2+��Cl-��SO42- |
| B��Mg2+��NH4+��Cl-��SO42- |
| C��Fe2+��H+��SO32-��ClO- |
| D��K+��Fe3+��NO3-��SCN- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ѧ������֮��Ĺ�ϵ��a��b+c |
| B������B�����������С |
| C��ƽ��������Ӧ�����ƶ� |
| D��ƽ���ƶ������У���ԭƽ�����v������v����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
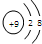 �����ӵ�˵������ȷ���ǣ�������
�����ӵ�˵������ȷ���ǣ�������| A���˵����Ϊ9 |
| B���������������Ӳ� |
| C������������ |
| D���ڻ�ѧ��Ӧ�����õ�1������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10mL��������Ϊ98%��H2SO4����ˮϡ����100mL��H2SO4��������������9.8% |
| B����H2O2+Cl2=2HCl+O2��Ӧ�У�ÿ����32g��������ת�Ƶ��Ӹ���Ϊ2moL |
| C����״���£�������ΪNA��CO��C2H4����������ԼΪ22.4L������Ϊ28g |
| D��ij��ɫ��Һ��ͨ��Cl2����Һ��Ϊ�ػ�ɫ���ټ��������Һ����Һ��Ϊ��ɫ��˵��ԭ��Һ�д���I- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1 mol NaHSO4������������������������Ϊ0.3 NA |
| B��22.4L NH3�к��е�ԭ������Ϊ4NA |
| C��1mol�������ڳ����»��ȼ��������O2��ȫ��Ӧת�Ƶĵ�������ΪNA |
| D�����������£������ʵ���Ũ�ȵ�HCl��Һ��NaOH��Һ��ϣ���ҺpH=7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1molCH4��Cl2����ȡ����Ӧ�������2molCl2 | ||
| B������������ˮ������ȡ����Ӧ | ||
C��CH3-CH�TCH2+Cl2
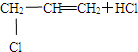 ���ڼӳɷ�Ӧ ���ڼӳɷ�Ӧ | ||
D���ױ����������������ױ��Ļ�ѧ����ʽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
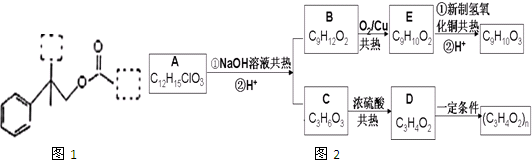
| HBr |
| NaOH |
| ˮ/�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
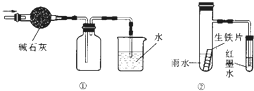
| A����ȡ��ˮ�е��壬���ü����Ҵ���ȡ�ķ��� |
| B���������ܼ��ķ�����10%���Ȼ�����Һ��Ϊ20%���Ȼ�����Һ |
| C����ͼ �ٵ�װ�ÿ����ռ�һƿ����İ��� |
| D����ͼ �ڵ�װ�ÿ�����֤����Ƭ�ڸ���ˮ���Ƿ�ᷢ��������ʴ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com