
【题目】下列关于ΔH-TΔS的说法中正确的是
A.ΔH-TΔS可用于判断所有条件下的反应能否自发进行
B.ΔH-TΔS只用于判断温度、体积一定的反应能否自发进行
C.ΔH-TΔS只用于判断温度、压强一定的反应能否自发进行
D.某反应ΔH-TΔS<0,则该条件下此反应一定剧烈进行
科目:高中化学 来源: 题型:
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH)。该反应的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是________。
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应。反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图,则上述CO2转化为甲醇的反应的△H_____0(填“>”、“<”、“=”)
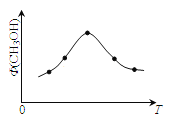
(3)上述反应在实际生产中采用的温度是300℃,其目的是_________________。
(4)300℃时,将CO2与H2按1∶3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图所示。回答问题:
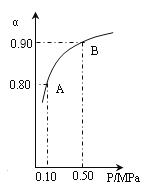
①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是_______。
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1∶3 D.H2的体积分数减小
②B点平衡混合气体的平均摩尔质量为_______________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有如下两个反应:①NaOH + HCl =" NaCl" + H2O;②Fe +H2SO4= FeSO4 + H2 ↑
两反应中为放热反应的是 ,能设计成原电池的是 。(填序号)
(2)根据下图填空①电子从 片流出,溶液中H+向 片移动。

② 正极的现象是 ,发生 反应(填写“氧化”或“还原”)。
③负极的电极方程式为
④ 若反应过程中有0.01mol电子发生转移,则生成的氢气在标准状况下的体积为 L。
(3)写出电解氯化铜溶液时,阴极的电极反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cr2O72-和CN-是工业废水中常见的污染物。若利用下列流程可对分别含两种离子的废水进行综合处理:

回答下列问题:
(1)已知步骤②中无气体生成,写出反应的离子方程式_______________,步骤④中NaClO可将CNO-处理为完全无害的溶液,该过程中有两种无毒的不支持燃烧的气体产生,写出这两种气体的化学式___________________。
(2)步骤⑥的反应为 S2O32-+ Cr2O72-+2H+→SO42-+ Cr3++H2O(未配平),则每处理1mol Cr2O72-离子转移_______mol电子。
(3)步骤⑦的操作名称为_______,该操作所需的玻璃仪器为____________。
(4)CrO42-和Cr2O72-在溶液中可相互转化,用离子方程式表示K2Cr2O7溶液中的转化反应_____。
(5)Cr3+也有一定毒性,会污染水体,常温下要除去废液中多余的Cr3+,调节pH至少为_______,才能使铬离子沉淀完全(铬离子浓度应小于10-5mol/L)。已知Cr(OH)3的溶度积为6.3×10-31, ![]() ≈4,lg2≈0.3。
≈4,lg2≈0.3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是![]() 在400-500℃下的催化氧化:
在400-500℃下的催化氧化:![]()
![]()
![]() , 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
, 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
A. 使用催化剂是为了加快反应速率,提高生产效率 B. 在上述条件下,![]() 不可能100%转化为
不可能100%转化为![]() C. 为提高
C. 为提高![]() 的转化率,应适当提高
的转化率,应适当提高![]() 的浓度 D. 达到平衡时,
的浓度 D. 达到平衡时,![]() 的浓度与
的浓度与![]() 的浓度相等
的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于判断过程方向的说法正确的是
A.所有自发进行的化学反应都是放热反应
B.高温、高压下可以使石墨转化为金刚石是自发的化学反应
C.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
D.同一物质的固、液、气三种状态的熵值相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.C2H4与C4H8一定是同系物
B.丙烯和乙烷都能使高锰酸钾酸性溶液褪色
C.1丁烯与2丁烯互为同分异构体
D.新戊烷和2,2二甲基丙烷互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1 mol/LNa2SO4溶液中,Na+的物质的量浓度是
A. 0.1 mol/LB. 0.2 mol/LC. 0.05mol/LD. 1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化镍在乙醇的悬浊液中可发生如下反应生成单质镍的配合物:
Ni(OH)2+5CH3NC=(CH3NC)4Ni +CH3NCO+H2O
⑴Ni2+基态核外电子排布式为___________。
⑵CH3NC(其结构简式为![]() )分子中碳原子轨道的杂化类型是___________;
)分子中碳原子轨道的杂化类型是___________;
 1 molCH3NC中σ键的数目为___________。
1 molCH3NC中σ键的数目为___________。
⑶用光气(COCl2)与甲胺(CH3NH2)可以制取CH3NCO。
①与COCl2互为等电子体的一种阴离子为___________。
②甲胺极易溶于水,除因为它们都是极性分子外,还因为___________。
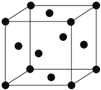
⑷Ni单质的晶胞结构如右图所示,每个晶胞中含Ni原子数目为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com