
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH)。该反应的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是________。
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
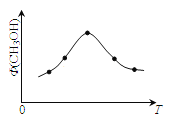
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应。反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图,则上述CO2转化为甲醇的反应的△H_____0(填“>”、“<”、“=”)
(3)上述反应在实际生产中采用的温度是300℃,其目的是_________________。
(4)300℃时,将CO2与H2按1∶3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图所示。回答问题:
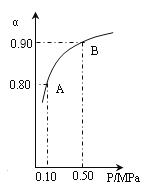
①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是_______。
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1∶3 D.H2的体积分数减小
②B点平衡混合气体的平均摩尔质量为_______________(保留一位小数)。
【答案】BC<加快反应速率,使催化剂活性最高CD22.7g/mol
【解析】
(1)根据平衡状态的含义分析;
(2)根据甲醇含量与温度关系分析;
(3)根据温度与反应速率和催化剂活性关系分析;
(4)①根据压强与反应速率及平衡关系分析;
②根据B点的平衡转化率为0.8结合平均相对分子质量的含义计算。
解析:(1)A.CO2和CH3OH的浓度相等不能说明正逆反应速率是否相等,不一定是平衡状态,A错误; B.H2的百分含量保持不变,说明是平衡状态,B正确;C.正反应体积减小,容器内压强保持不变 ,说明是平衡状态,C正确;D.3v正(H2)=v逆(H2O) 不满足反应速率之比是相应的化学计量数之比,因此没有达到平衡状态,D错误;E.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此容器中混合气体的密度保持不变不能说明反应达到平衡状态,E错误,答案选BC;
(2)随着温度的升高甲醇含量增加,反应向正反应方向进行;达到最高后说明达到平衡状态,继续升高温度甲醇含量降低,说明升高温度平衡向逆反应方向进行,正反应是放热反应;
(3)采用300℃的温度,可以加快反应速率,且催化剂活性较高;
(4)合成塔中发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
①A.体积压缩,反应混合物各组分浓度均增大,A错误;B.体积压缩,压强增大,正、逆反应速率都增大,B错误;C.CO2和H2按1:3的体积比投入,且二者按物质的量1:3反应,反应体系中CO2和H2的体积比始终为1:3,C正确;D.压缩体积,增大压强,平衡正向移动,氢气的体积分数减小,D正确,答案选CD;
②设CO2和H2分别是1mol、3mol。由图可知,0.5MPa条件下CO2的平衡转化率为0.9,可知反应的CO2为0.9mol,根据方程式可知参加反应氢气物质的量为0.9mol×3=2.7mol,生成甲醇和水蒸气分别是0.9mol、0.9mol,所以混合气体的平均摩尔质量是![]() 。
。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中立刻泛起大量泡沫
B. 由H2、I2蒸气、HI组成的平衡混合物加压后颜色变深
C. 向氯水中加适量NaHCO3后,溶液漂白能力增强
D. 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA为阿伏加德罗常数)( )
A. 124 g P4含有P—P键的个数为4NA
B. 60gSiO2中含Si—O键的个数为2NA
C. 12 g石墨中含有C—C键的个数为1.5NA
D. 36 g戊烷中共价键的个数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在人类生活中扮演着重要角色,下列应用不正确的是( )
A.明矾可用于水的杀菌,消毒
B.盐卤可用于制豆腐
C.目前加碘食盐主要添加的是KIO3
D.在空气质量日报中SO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.02molL-1MOH溶液滴定100mL0.01molL-1HA溶液,右图为加入MOH溶液的体积与混合溶液的pH变化情况(溶液体积变化勿略不计)。

回答下列问题:
(1)由图中信息可知HA为_____酸(填“强”或“弱”),滴定所用的最适宜指示剂为______,滴定时眼睛注视__________________。
(2)常温下一定浓度的MA稀溶液的pH=a,则a_____7(填“大于”、“小于”或“等于”)此时,溶液中水电离出的c(OH-)=__________。
(3)请写出K点所对应的溶液中离子浓度的由大到小的关系:_______________。
(4)K点所对应的溶液中,c(M+)+c(MOH)______2c(A-)。(填“大于”“小于”“等于”)
(5)室温下MOH溶液加水稀释过程中,下列数值变小的是_______________(填序号)
①C(H+) ② C(H+)/ C(OH-) ③ C(OH-) ④ C(OH-)/ C(M+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于CH4和CO2的说法正确的是
A. 固态CO2属于原子晶体
B. CH4分子中含有极性共价键,是极性分子
C. 因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
D. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学电池的说法中正确的是
A.化学电池只能将化学能转化为电能
B.燃料电池能将全部化学能转化为电能
C.锌银电池比能量大,电压稳定,储存时间长
D.一次电池包括干电池和蓄电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于ΔH-TΔS的说法中正确的是
A.ΔH-TΔS可用于判断所有条件下的反应能否自发进行
B.ΔH-TΔS只用于判断温度、体积一定的反应能否自发进行
C.ΔH-TΔS只用于判断温度、压强一定的反应能否自发进行
D.某反应ΔH-TΔS<0,则该条件下此反应一定剧烈进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com