
【题目】下列说法正确的是(NA为阿伏加德罗常数)( )
A. 124 g P4含有P—P键的个数为4NA
B. 60gSiO2中含Si—O键的个数为2NA
C. 12 g石墨中含有C—C键的个数为1.5NA
D. 36 g戊烷中共价键的个数为10NA
【答案】C
【解析】A.n(P4)= ![]() =
=![]() =1mol,1个P4分子含有6个P-P键,因此124g P4含有的P-P键的物质的量为6mol,P-P键的个数为6NA,故A错误;B.n(SiO2)=
=1mol,1个P4分子含有6个P-P键,因此124g P4含有的P-P键的物质的量为6mol,P-P键的个数为6NA,故A错误;B.n(SiO2)= ![]() =
=![]() =1mol,在二氧化硅晶体中,每个硅原子形成4个Si-O键,因此60gSiO2中含Si-O键的物质的量为4mol,Si-O键的个数为4NA,故B错误;C.12g石墨中含有碳原子的物质的量n=
=1mol,在二氧化硅晶体中,每个硅原子形成4个Si-O键,因此60gSiO2中含Si-O键的物质的量为4mol,Si-O键的个数为4NA,故B错误;C.12g石墨中含有碳原子的物质的量n=![]() =
=![]() ==1mol,在石墨晶体中一个碳原子形成3个C-C键,每个C-C键由2个碳原子构成,因此12g石墨中含有C-C键的物质的量为1mol×3×
==1mol,在石墨晶体中一个碳原子形成3个C-C键,每个C-C键由2个碳原子构成,因此12g石墨中含有C-C键的物质的量为1mol×3×![]() =1.5mol,C-C键的个数为1.5NA,故C正确;D.每个戊烷分子中含有16个共价键,36 g戊烷的物质的量为0.5mol,含有共价键的个数为8NA,故D错误;答案为C。
=1.5mol,C-C键的个数为1.5NA,故C正确;D.每个戊烷分子中含有16个共价键,36 g戊烷的物质的量为0.5mol,含有共价键的个数为8NA,故D错误;答案为C。


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g) ![]() 2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是( )
2C(g),2 min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果正确的是( )
A. 平衡时,物质的量之比n(A)∶n(B)∶n(C)=2∶11∶4
B. x值等于3
C. A的转化率为20%
D. B的平均反应速率为0.4 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A.p(H2)>p(Ne)>p(O2) B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne) D.p(Ne)>p(H2)>p(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若某基态原子的外围电子排布为3d14s2,则下列说法正确的是( )
A. 该元素属于P区B. 该元素原子核外有4个电子层
C. 该元素原子最外层共有3个电子D. 该元素原子M能层共有8个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关.下列说法正确的是( )
A.石油分馏的目的是获得乙烯、丙烯和丁二烯
B.减少SO2的排放,可以从根本上消除雾霾
C.食品工业利用液态二氧化碳代替有机溶剂,能避免有机溶剂污染食品
D.蔬菜表面洒少许福尔马林,可保鲜和消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能够用键能解释的是
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液体,碘为固体
C.稀有气体一般很难发生化学反应
D.硝酸易挥发,硫酸难挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中正确的是
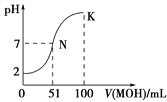
A. MOH为一元强碱
B. K点对应的溶液中:c(M+) + c(MOH) = c(A-)
C. K点对应的溶液中:c(MOH)+c(OH-)-c (H+)=0.005 mol·L-1
D. N点水的电离程度小于K点水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH)。该反应的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是________。
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应。反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图,则上述CO2转化为甲醇的反应的△H_____0(填“>”、“<”、“=”)
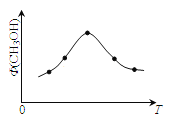
(3)上述反应在实际生产中采用的温度是300℃,其目的是_________________。
(4)300℃时,将CO2与H2按1∶3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图所示。回答问题:
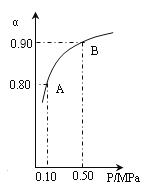
①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是_______。
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1∶3 D.H2的体积分数减小
②B点平衡混合气体的平均摩尔质量为_______________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有如下两个反应:①NaOH + HCl =" NaCl" + H2O;②Fe +H2SO4= FeSO4 + H2 ↑
两反应中为放热反应的是 ,能设计成原电池的是 。(填序号)
(2)根据下图填空①电子从 片流出,溶液中H+向 片移动。

② 正极的现象是 ,发生 反应(填写“氧化”或“还原”)。
③负极的电极方程式为
④ 若反应过程中有0.01mol电子发生转移,则生成的氢气在标准状况下的体积为 L。
(3)写出电解氯化铜溶液时,阴极的电极反应方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com