
【题目】常温下,用0.02molL-1MOH溶液滴定100mL0.01molL-1HA溶液,右图为加入MOH溶液的体积与混合溶液的pH变化情况(溶液体积变化勿略不计)。

回答下列问题:
(1)由图中信息可知HA为_____酸(填“强”或“弱”),滴定所用的最适宜指示剂为______,滴定时眼睛注视__________________。
(2)常温下一定浓度的MA稀溶液的pH=a,则a_____7(填“大于”、“小于”或“等于”)此时,溶液中水电离出的c(OH-)=__________。
(3)请写出K点所对应的溶液中离子浓度的由大到小的关系:_______________。
(4)K点所对应的溶液中,c(M+)+c(MOH)______2c(A-)。(填“大于”“小于”“等于”)
(5)室温下MOH溶液加水稀释过程中,下列数值变小的是_______________(填序号)
①C(H+) ② C(H+)/ C(OH-) ③ C(OH-) ④ C(OH-)/ C(M+)
【答案】 强 甲基橙 锥形瓶内颜色变化 小于 ![]()
![]() 等于 ③
等于 ③
【解析】(1)根据图象知,0.01molL-1HA溶液中PH=2,氢离子浓度等于酸浓度,所以该酸是强酸;50ml碱溶液恰好反应后,溶液呈酸性,51ml恰好溶液呈中性,说明碱为弱碱,故滴定所用的最适宜指示剂为甲基橙,滴定操作时眼睛注视锥形瓶内颜色变化;
(2)N点时溶液呈中性,MOH的物质的量大于HA的物质的量,说明MOH是弱碱,MA属于强酸弱碱盐,水解显示酸性,即a<7;因M++H2OMOH+H+,则溶液中的H+来源于水的电离,且水电离的H+和OH-浓度相等,即溶液中水电离出的c(OH-)=c(H+)=![]() ;
;
(3)在K点时混合溶液体积是碱溶液的2倍,溶液pH>7,溶液显示碱性,则c(OH-)>c(H+),根据电荷守恒c(OH-)+c(OH-)=c(H+)+c(M+)可得,c(M+)>c(A-),溶液中各离子浓度大小为:c(M+)>c(A-)>c(OH-)>c(H+);
(4)K点时,加入的MOH的物质的量=0.02molL-1×0.1L=0.002mol,混合溶液的体积是0.2L,根据物料守恒知,c(M+)+c(MOH)= ![]() =0.01mol/L,HA是强酸,所以反应后的溶液中,c(A-)=
=0.01mol/L,HA是强酸,所以反应后的溶液中,c(A-)=![]() ×0.01molL-1=0.005molL-1,故c(M+)+c(MOH)=2c(A-);
×0.01molL-1=0.005molL-1,故c(M+)+c(MOH)=2c(A-);
(5)加水促进MOH的电离,电离出的OH-离子的物质的量增大,但由于溶液体积增大,故溶液中OH-离子浓度减小,水的离子积常数不变,则C(H+) 增大,故①错、③正确;同时C(H+)/ C(OH-) 比值增大,②错误; MOH溶液加水稀释过程中,OH-、M+最初均来源于MOH的电离,C(OH-)与C(M+)基本相等,当无限稀释时,OH-主要来之于水的电离,则C(OH-)/ C(M+)先变小后变大,故错误,答案为③。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式如图所示.有关该化合物的叙述不正确的是( )

A. 该有机物的分子式为C11H12O2
B. 1mol该物质最多能与4mol H2发生加成反应
C. 该有机物在一定条件下,可以发生取代、氧化、酯化反应
D. 该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关.下列说法正确的是( )
A.石油分馏的目的是获得乙烯、丙烯和丁二烯
B.减少SO2的排放,可以从根本上消除雾霾
C.食品工业利用液态二氧化碳代替有机溶剂,能避免有机溶剂污染食品
D.蔬菜表面洒少许福尔马林,可保鲜和消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中正确的是
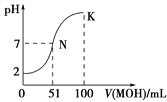
A. MOH为一元强碱
B. K点对应的溶液中:c(M+) + c(MOH) = c(A-)
C. K点对应的溶液中:c(MOH)+c(OH-)-c (H+)=0.005 mol·L-1
D. N点水的电离程度小于K点水的电离程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现C60 后,近年又合成了许多球形分子(富勒烯),如C50 、C70 、C120 、C540 等,它们互称为 ( )
A. 同系物 B. 同分异构体 C. 同素异形体 D. 同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家提出“绿色自由”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH)。该反应的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H
CH3OH(g)+H2O(g) △H
(1)若在一个定温定容的容器中发生上述反应,反应达到平衡的标志是________。
A.CO2和CH3OH的浓度相等
B.H2的百分含量保持不变
C.容器内压强保持不变
D.3v正(H2)=v逆(H2O)
E.容器中混合气体的密度保持不变
(2)若将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应。反应相同时间后,测得甲醇的体积分数 (CH3OH)与反应温度T的关系如图,则上述CO2转化为甲醇的反应的△H_____0(填“>”、“<”、“=”)
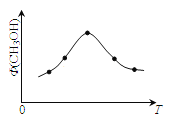
(3)上述反应在实际生产中采用的温度是300℃,其目的是_________________。
(4)300℃时,将CO2与H2按1∶3的体积比充入某密闭容器中,CO2的平衡转化率(a)与体系总压强(P)的关系如图所示。回答问题:
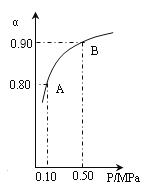
①若其他条件不变,将A点的体积压缩至原来的一半,一段时间后反应再次达到平衡,与原平衡相比较下列说法正确的是_______。
A.CO2的浓度减小 B.正反应速率增大,逆反应速率减小
C.CO2和H2的体积比仍然是1∶3 D.H2的体积分数减小
②B点平衡混合气体的平均摩尔质量为_______________(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,完成下列问题:

(1)干电池放电时负极发生的电极方程式为____________________。
(2)氢氧燃料电池在酸性电解质环境中放电时氢气在______(填“正”或“负”)极发生______反应(填“氧化”或“还原”),电路中每转移0.4mol电子,标准状况下消耗O2的体积是______L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图,下列说法正确的是( )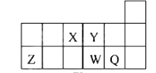
A. 元素X与元素Z的最高正化合价之和的数值等于8
B. 原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W) >r(Q)
C. 离子Y2-和Z 3+的核外电子数和电子层数都不相同
D. 元素W的最高价氧化物对应的水化物的酸性比Q的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是![]() 在400-500℃下的催化氧化:
在400-500℃下的催化氧化:![]()
![]()
![]() , 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
, 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
A. 使用催化剂是为了加快反应速率,提高生产效率 B. 在上述条件下,![]() 不可能100%转化为
不可能100%转化为![]() C. 为提高
C. 为提高![]() 的转化率,应适当提高
的转化率,应适当提高![]() 的浓度 D. 达到平衡时,
的浓度 D. 达到平衡时,![]() 的浓度与
的浓度与![]() 的浓度相等
的浓度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com