
【题目】科学家发现C60 后,近年又合成了许多球形分子(富勒烯),如C50 、C70 、C120 、C540 等,它们互称为 ( )
A. 同系物 B. 同分异构体 C. 同素异形体 D. 同位素
科目:高中化学 来源: 题型:
【题目】按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物—酸—碱—盐”顺序排列的是( )
A.CO HNO3 NaOH KNO3
B.CO2 H2CO3 Na2CO3 Ca(HCO3)2
C.H2SO4 HCl Mg(OH)2 MgCl2
D.SO3 NaHCO3 NaOH Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是:( )
A. SO2、SO3都是极性分子
B. 在 [Cu(NH3)4]2+中存在配位键而NH4+中不存在配位键
C. 元素电负性越大的原子,吸引电子的能力越强
D. 物质的沸点按HF、HCl、HBr、HI的顺序依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重庆天原化工总厂的氯气贮罐发生泄漏,严重影响了附近群众的生命安全。下列有关安全措施中不正确的是
A.可用毛巾蘸取石灰水捂嘴 B.在氯气泄漏的地区人应站在高处
C.向氯气中喷洒水 D.将泄漏的氯气在空气中点燃除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.02molL-1MOH溶液滴定100mL0.01molL-1HA溶液,右图为加入MOH溶液的体积与混合溶液的pH变化情况(溶液体积变化勿略不计)。

回答下列问题:
(1)由图中信息可知HA为_____酸(填“强”或“弱”),滴定所用的最适宜指示剂为______,滴定时眼睛注视__________________。
(2)常温下一定浓度的MA稀溶液的pH=a,则a_____7(填“大于”、“小于”或“等于”)此时,溶液中水电离出的c(OH-)=__________。
(3)请写出K点所对应的溶液中离子浓度的由大到小的关系:_______________。
(4)K点所对应的溶液中,c(M+)+c(MOH)______2c(A-)。(填“大于”“小于”“等于”)
(5)室温下MOH溶液加水稀释过程中,下列数值变小的是_______________(填序号)
①C(H+) ② C(H+)/ C(OH-) ③ C(OH-) ④ C(OH-)/ C(M+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)的单质和化合物在化工生产等方面具有重要应用。
(1)下列关于碲及其化合物的叙述不正确的是_______。
A.Te位于元素周期表的第五周期ⅣA族
B. Te的氧化物通常有TeO2和TeO3
C. H2TeO4的酸性比H2SO4酸性强
D.热稳定性H2Te比H2S弱,H2Te比HI强
(2)25℃时,亚碲酸(H2TeO3)的 ![]() = 1×10-3,
= 1×10-3, ![]() =2×10-8。0. 1 mol . L-1H2TeO3 的电离度 a 约为___________ (
=2×10-8。0. 1 mol . L-1H2TeO3 的电离度 a 约为___________ (![]() ); NaHTeO3的溶液的pH_______7(填“>”、“=”或“<”)。
); NaHTeO3的溶液的pH_______7(填“>”、“=”或“<”)。
(3)TeO2微溶于水,易溶于较浓的强酸和强碱。工业上常用铜阳极泥(主要含有TeO2、少量Ag、Au)为原料制备单质碲,其工艺流程如下:
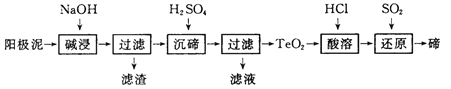
①“碱浸”时TeO2发生反应的化学方程式为 _________。
②“沉碲”时控制溶液的pH为4. 5~5. 0,生成Tea沉淀。酸性不能过强的原因是_________;防止局部酸度过大的操作方法是____________。
③“酸溶”后,将SO2通入TeCl4酸性溶液中进行“还原”得到碲,该反应的化学方程式是____________。
④工业上还可以通过电解铜阳极泥碱浸、过滤后的滤液得到单质碲。已知电解时的电极均为石墨,则阴极的电极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
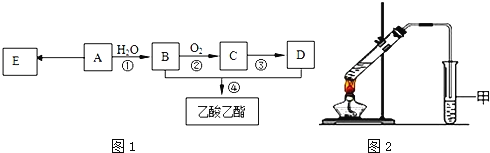
(1)A分子中官能团的名称是______,D中官能团的名称是______;反应①的反应类型是______反应.
(2)反应②的化学方程式是______,反应④的化学方程式是______.
(3)E是常见的高分子材料,合成E的化学方程式是______.
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的目的是______.
②上述实验中饱和碳酸钠溶液的作用是(填字母)______.
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.加速酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
A.v(O2)=0.01mol/(L·s) B.v(NO)=0.08mol/(L·s)
C.v(H2O)=0.003mol/(L·s) D.v(NH3)=0.001mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com