
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
4NO(g)+6H2O(g)在5L密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率v为
A.v(O2)=0.01mol/(L·s) B.v(NO)=0.08mol/(L·s)
C.v(H2O)=0.003mol/(L·s) D.v(NH3)=0.001mol/(L·s)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】科学家发现C60 后,近年又合成了许多球形分子(富勒烯),如C50 、C70 、C120 、C540 等,它们互称为 ( )
A. 同系物 B. 同分异构体 C. 同素异形体 D. 同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是4个碳原子相互结合形成的8种有机物(氢原子没有画出)A-H(据此回答下列各题)

(1)有机物E的名称是 (_____)
A.丁烷 B.2-甲基丙烷 C.1-甲基丙烷 D.甲烷
(2)有机物B、C、D互为 (_____)
A.同位素 B.同系物 C.同分异构体 D.同素异形体
(3)每个碳原子都跟两个氢原子通过共价键结合的有机物是(______)
A.B B.F C.G D.H
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于硫酸工业中SO2的催化氧化反应 2SO2+O2![]() 2SO3,下列说法错误的是( )
2SO3,下列说法错误的是( )
A.使用催化剂能加快化学反应速率
B.增大O2浓度可以使SO2转化率达到100%
C.降低反应温度,化学反应速率减慢
D.增大O2浓度,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.根据下列叙述写出相应的热化学方程式:
(1)已知16 g固体硫完全燃烧时放出148.4 kJ的热量,该反应的热化学方程式是__________________________。
(2)下图是198 K时N2与H2反应过程中能量变化的曲线图。
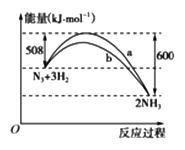
该反应的热化学方程式为:_____________________。
(3)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下1 g甲硅烷自燃放出热量44.6 kJ,其热化学方程式是___________________。
II.
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是_____________________。
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸中的一步重要反应是![]() 在400-500℃下的催化氧化:
在400-500℃下的催化氧化:![]()
![]()
![]() , 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
, 这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述相关说法中错误的是( )
A. 使用催化剂是为了加快反应速率,提高生产效率 B. 在上述条件下,![]() 不可能100%转化为
不可能100%转化为![]() C. 为提高
C. 为提高![]() 的转化率,应适当提高
的转化率,应适当提高![]() 的浓度 D. 达到平衡时,
的浓度 D. 达到平衡时,![]() 的浓度与
的浓度与![]() 的浓度相等
的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关自发反应的说法中正确的是
A.自发反应一定是ΔS > 0的反应
B.自发反应一定是ΔH < 0的反应
C.自发反应在任何条件下都能自动进行
D.ΔH < 0,ΔS > 0的反应一定是自发反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是

A. 该反应过程中的能量变化如图所示
B. 该反应条件下,Al的还原性弱于Fe
C. 1molFe3O4参与反应转移8×6.02×1023个电子
D. 实验室进行该反应时常加入KClO3作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物X的结构简式为 ,下列有关叙述不正确的是 ( )
,下列有关叙述不正确的是 ( )
A. 1 mol X分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别为3 mol、4 mol、1 mol
B. X在一定条件下能与FeCl3溶液发生显色反应
C. X在一定条件下能发生消去反应和酯化反应
D. X的化学式为C10H10O6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com