
【题目】晶体硅是制备太阳能电池板的主要原料,电池板中还含有硼、氮、钛、钻、钙等多种化学物质。请回答下列问题:
(1)科学家常利用X-射线衍射实验区分晶体硼和无定形硼,二者之关的关系互为_________。第二周期元素的第一电离能按由小到大的顺序排列,B元素排在第____位,其基态能量最低的能极电子云轮廊图为____________。
(2)硅酸根有多种结构形式,一种无限长链状结构如图1所示,其化学式为_______,Si原子的杂化类型为__________________。
(3)N元素位于元素周期表___________区;该元素形成的氢化物的沸点比同族元素的氢化物沸点高,其原因为____________________________________________________。

(4)[Co(NH3)6]3+的几何构型为正八面体形,Co在中心。[Co(NH3)6]3+中,1个Co提供___个空轨道。该配位离子的作用力为_________________(填序号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
(5)一种由Ca、Ti、O三种元素形成的晶体的立方晶胞结构如图2所示。
①与Ti紧邻的Ca有________________个。
②若Ca与O之间的最短距离为a pm,阿伏加德罗常数的值为NA,则晶体的密度ρ=___g cm-3(用含a、NA的代数式表示)。
【答案】 同素异形体 2 球形 SiO32- [或(SiO3)n2n-] sp3 p 氨分子间存在氢键,同族其他氢化物只有范德华力 6 CD 8 ![]() 或
或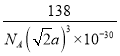
【解析】试题分析:(1) 晶体硼和无定形硼是硼元素组成的不同单质;同周期元素的第一电离能从左到右依次增大,但铍原子2S轨道全充满,第一电离能大于相邻的硼原子;硼原子基态时能量最低的能级为1s;(2)根据图1,每个硅原子与4个O原子成键,4个O原子中有2个O原子被2个硅原子共用;(3)N原子核外电子排布式是![]() ;氨分子间能形成氢键;1个Co原子与6个NH3分子形成配位键;(5)①由于1个顶点可以形成8个立方体,所以根据晶胞结构可知,在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钙离子有8个;根据均摊法计算该晶体的化学式,根据
;氨分子间能形成氢键;1个Co原子与6个NH3分子形成配位键;(5)①由于1个顶点可以形成8个立方体,所以根据晶胞结构可知,在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钙离子有8个;根据均摊法计算该晶体的化学式,根据![]() 计算密度;
计算密度;
解析:(1) 晶体硼和无定形硼是硼元素组成的不同单质,所以晶体硼和无定形硼之关的关系互为同素异形体;同周期元素的第一电离能从左到右依次增大,但铍原子2S轨道全充满,第一电离能大于相邻的硼原子,所以硼的第一电离能仅大于锂,第一电离能按由小到大的顺序排列,B元素排在第2位;其基态能量最低的能级为1s,电子云轮廊图为球形;(2)根据图1,每个硅原子与4个O原子成键,4个O原子中有2个O原子被2个硅原子共用,实际每个硅原子占用氧原子数![]() ,化学式为SiO32-,Si原子的杂化类型为sp3;(3)N原子核外电子排布式是
,化学式为SiO32-,Si原子的杂化类型为sp3;(3)N原子核外电子排布式是![]() ,最外能层是2p,所以N元素位于元素周期表p区;氨分子间能形成氢键,同族其他氢化物只有范德华力,所以氨气的沸点比同族元素的氢化物沸点高;1个Co原子与6个NH3分子形成配位键,1个Co提供6个空轨道。该配位离子的作用力为配位键、共价键;(5)①由于1个顶点可以形成8个立方体,所以根据晶胞结构可知,在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钙离子有8个;根据均摊法,每个晶胞含有Ca、Ti、O原子数1、
,最外能层是2p,所以N元素位于元素周期表p区;氨分子间能形成氢键,同族其他氢化物只有范德华力,所以氨气的沸点比同族元素的氢化物沸点高;1个Co原子与6个NH3分子形成配位键,1个Co提供6个空轨道。该配位离子的作用力为配位键、共价键;(5)①由于1个顶点可以形成8个立方体,所以根据晶胞结构可知,在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钙离子有8个;根据均摊法,每个晶胞含有Ca、Ti、O原子数1、![]() 、
、![]() ,该晶体的化学式是CaTiO3,晶胞的摩尔质量是138g/mol, 1个晶胞的质量是
,该晶体的化学式是CaTiO3,晶胞的摩尔质量是138g/mol, 1个晶胞的质量是![]() g,Ca与O之间的最短距离为a pm,则晶胞的边长是
g,Ca与O之间的最短距离为a pm,则晶胞的边长是![]() ,
, ![]() ,
, 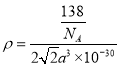 =
= ![]() ;
;


科目:高中化学 来源: 题型:
【题目】2014年5月21日,中俄签订了30年天然气供应合同,成为我国得到清洁能源的主要来源。天然气的主要成分是
A. CH4 B. CO2 C. CO D. H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应Na2CO3+2HCl=2NaCl+H2O+CO2↑的离子方程式是
A. CO32-+2H+=H2O+CO2↑
B. CO32-+H+=H2O+CO2↑
C. CO32-+2HCl=2Cl-+H2O+CO2↑
D. Na2CO3+2H+=2Na++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】—定温度下,将2 mol SO2和1mol O2充入10 L恒容密闭容器中,发生反应2SO2(g) +O2(g)![]() 2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
2SO3(g) △H =-196 kJ mol-1。5 min时达到平衡,测得反应放热166. 6 kJ。下列说法错误的是
A. 0~5 min内,用O2表示的平均反应速率V(O2)=0.017 mol·L-1·min-1
B. ![]() 的值不变时,该反应达到平衡状态
的值不变时,该反应达到平衡状态
C. 若增大O2的浓度,SO2的转化率增大
D. 条件不变,若起始时充入4 mol SO2和2 mol O2,平衡时放出的热量小于333.2 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 50 g 46%的乙醇水溶液中含有的氢原子总数为3NA
B. 1 mol H2与足量O2反应生成的H2O中含有的共价键总数为2NA
C. 0.1molSO2溶于水,溶液中SO32-、HSO3-、H2SO3的总数为0.1NA
D. 用铂电极电解100 mL 1 mol L-1的CuSO4溶液足够长时间,转移的电子数一定为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构为 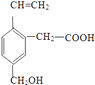 ,这种有机物不可能具有的性质是( )
,这种有机物不可能具有的性质是( )
A.能跟NaOH溶液反应
B.能使酸性KMnO4溶液褪色
C.能发生酯化反应
D.能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时H2S饱和溶液1 L,其浓度为0.1 mol·L-1,其电离方程式为H2S![]() H++HS-,HS-
H++HS-,HS-![]() H++S2-,若要使该溶液c(H+)及c(S2-)都减少,可采取的措施是( )
H++S2-,若要使该溶液c(H+)及c(S2-)都减少,可采取的措施是( )
A. 加入适量的稀硫酸
B. 加入适量的NaOH固体
C. 通入适量的SO2
D. 加入适量的CuSO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,下列说法正确的是( ) 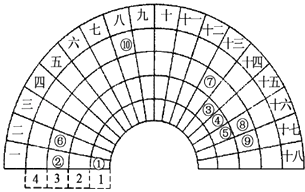
A.②、⑧、⑨对应简单离子半径依次减小
B.⑤的三种核素化学性质不同
C.元素=10 ⑩处于常见周期表第四周期第VIIIB族
D.④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示:用两张圆形滤纸分别折叠成漏斗状,套在一起,使四周都有四层.把内层滤纸取出,在底部剪一个小孔,用水润湿,再跟另一纸漏斗套在一起,架在铁圈上,下面放置一盛沙的蒸发皿.把5g干燥的氧化铁粉末和2g铝粉混合均匀,放在纸漏斗中,上面加少量氯酸钾并在混合物中间插一根镁条,用小木条点燃镁条.观察发生的现象.通过以上实验信息,回答下列问题: 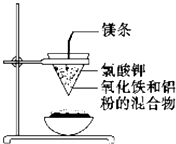
(1)写出该反应的化学方程式: , 该反应称为反应.
(2)选出该实验的实验现象(填写在横线上): .
①镁条剧烈燃烧
②放出大量的热,并发出耀眼的光芒,火星四射
③纸漏斗的下部被烧穿
④有红热状态的液珠落入蒸发皿内的细沙上,液珠冷却后变为黑色固体
(3)写出各物质的作用:蒸发皿盛沙:;镁条:;氯酸钾: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com