
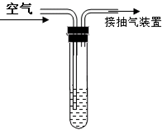
 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 级别 | 一级指标 | 二级指标 | 三级指标 |
| 浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
分析 根据反应的化学方程式,由恰好完全反应消耗碘的质量计算出1m3空气中所含二氧化硫的质量,转化为标准表示法mg/m3,与级别标准对比,判断出空气中二氧化硫的浓度级别.
解答 解:设1m3的空气中含有二氧化硫的质量为x
SO2+I2+2H2O=H2SO4+2HI
64 254
x 1.27mg
$\frac{64}{x}=\frac{254}{1.27mg}$
x=0.32mg
此空气中二氧化硫的最高浓度0.32mg/m3
因为0.15mg/m3<0.32mg/m3<0.50 mg/m3
所以该地区空气中二氧化硫的浓度级别为二级.
答:该地区空气中二氧化硫的浓度级别为二级.
点评 本题为根据化学方程式的基本计算,在最后与级别标准对比时要注意:根据化学方程式计算所得值为空气中二氧化硫的质量,还需要转换成标准值.


科目:高中化学 来源: 题型:选择题
| A. | 0.4mol | B. | 0.5mol | C. | 0.8mol | D. | 1.6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气有广泛的来源 | B. | 氢气燃烧时放热多 | ||
| C. | 氢气比空气轻 | D. | 氢气燃烧后生成的水不污染空气 |
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:实验题
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
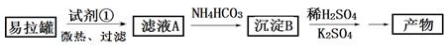
(1)为尽量少引入杂质,试剂①应选用 (填标号)。
A.HCl溶液 B.H2SO4溶液 C.氨水 D.NaOH溶液
(2)生成沉淀B的离子方程式为 ;明矾能用于净水,其原因是 ;往明矾溶液中滴加Ba(OH)2溶液,恰好使溶液中的SO42-完全沉淀的离子方程式为 。
。
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:推断题
A、B、C、D、E是中学常见的五种化合物,它们之间有下列转化关系:

已知A溶液显碱性,可促进水的电离;D溶液显酸性,A、D溶液焰色反应均为黄色。
(1)若A、B、C中含有相同的金属元素,且B能溶于酸也能溶于碱,D能与Ba(OH)2反应生成不溶于盐酸的白色沉淀。则A的化学式为 ,D的化学式为 ;A、C反应生成B的离子方程式为 。
(2)若C是一种无色无味的气体,且能使澄清石灰水变浑浊。用离子方程式表示A溶液显碱性的原因 ; C与E反应生成B的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ.
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个固定容积的密闭容器中充入1mol N2和3mol H2使反应N2(g)+3H2(g)?2NH3(g)达到平衡,测得反应放出热量为Q1kJ.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O2、KCl、CuSO4、NaNO3四种固体 | |
| B. | CCl4、乙醇、苯三种液体 | |
| C. | CaCO3、NaHSO4、Al2S3、Mg(OH)2四种固体 | |
| D. | NaCl、Na2SO4、AlCl3、MnO2四种固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com