
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
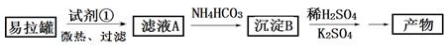
(1)为尽量少引入杂质,试剂①应选用 (填标号)。
A.HCl溶液 B.H2SO4溶液 C.氨水 D.NaOH溶液
(2)生成沉淀B的离子方程式为 ;明矾能用于净水,其原因是 ;往明矾溶液中滴加Ba(OH)2溶液,恰好使溶液中的SO42-完全沉淀的离子方程式为 。
。
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应一定有氧元素参加 | |
| B. | 氧化还原反应的本质是电子的转移 | |
| C. | 物质中某元素失去电子,则此物质是氧化剂 | |
| D. | 某一反应中有元素化合价的变化,则该反应不一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入明矾可以起到净水作用 | |
| B. | 热糖水降低温度后有固体析出,则原热糖水一定是饱和溶液 | |
| C. | 配制溶液时搅拌可以增大溶质的溶解度 | |
| D. | 物质溶于水时不会放出热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 火星大气中氮气的体积分数小于地球空气中氮气的体积分数 | |
| B. | 火星大气中二氧化碳的体积分数小于地球空气中二氧化碳的体积分数 | |
| C. | 火星大气中氧气的体积分数大于地球空气中氧气的体积分数 | |
| D. | 火星大气中有稀有气体,地球空气中没有 |
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:实验题
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为__ 。
(2)乙组同学认为甲组的实验不够严谨,该组同学在2mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是 。
(3)丙组同学取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二只试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是 (填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有 (填离子符号) ,由此可以证明该氧化还原反应为 反应(填“可逆”或“不可逆”)。
,由此可以证明该氧化还原反应为 反应(填“可逆”或“不可逆”)。
(4)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 ;一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
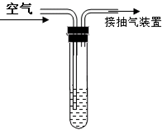 二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 级别 | 一级指标 | 二级指标 | 三级指标 |
| 浓度限值(mg/m3) | 0.15 | 0.50 | 0.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
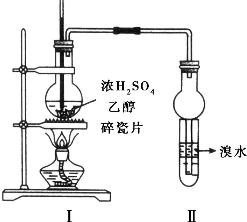 实验室制取乙烯的装置如图所示,试回答:
实验室制取乙烯的装置如图所示,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

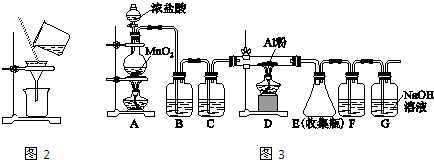
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com