
【题目】化合物H溴丙胺太林(普鲁本辛)属于抗胆碱类药物,用于胃和十二指肠溃疡的辅助治疗,亦用于胃炎、胰腺炎。某合成路线如下:
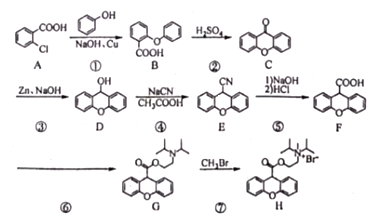
回答下列问题:
(1)A的化学名称为__________,E的分子式为__________________。
(2)①的反应类型为_____________。
(3)反应⑥的化学方程式为________________________________________________。
(4)H中含氧官能团的名称是_____________。
(5)N是D的同分异构体,含有联苯(![]() )结构,可与银氨溶液发生银镜反应,与
)结构,可与银氨溶液发生银镜反应,与![]() 溶液发生显色反应。符合该条件的D共有___________种;其中核磁共振氢谱为六组,峰面积比为1:2:2:2:2:1的结构简式为____________________________。
溶液发生显色反应。符合该条件的D共有___________种;其中核磁共振氢谱为六组,峰面积比为1:2:2:2:2:1的结构简式为____________________________。
(6)苯乙酸乙酯为合成香料,用于配制各种花香型日用香精。其一种合成路线为:

条件a为__________________,最后一步反应,乙醇稍过量的目的是______________。
【答案】邻氯苯甲酸或2-氯苯甲酸 ![]() 取代反应
取代反应 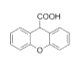 +HOCH2CH2N[CH(CH3)2]2
+HOCH2CH2N[CH(CH3)2]2![]()
 +H2O 酯基,醚键 19种
+H2O 酯基,醚键 19种 ![]() NaCN、
NaCN、![]() 使苯乙酸充分反应,提高苯乙酸的转化率
使苯乙酸充分反应,提高苯乙酸的转化率
【解析】
(1)根据有机物的系统命名法及A的结构简式对A进行命名;根据结构简式判断E的分子式;
(2)根据转化关系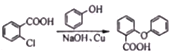 由物质转化判断反应类型;
由物质转化判断反应类型;
(3)反应⑥完成![]() →
→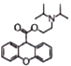 的转化,由F与
的转化,由F与![]() 发生酯化反应生成G;
发生酯化反应生成G;
(4)根据结构简式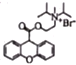 判断含氧官能团的名称;
判断含氧官能团的名称;
(5)根据所给条件确定同分异构体的数目及符合条件的同分异构体的结构简式;
(6)根据流程中物质转化进行分析。
(1)A为![]() ,化学名称为邻氯苯甲酸或2-氯苯甲酸,E为
,化学名称为邻氯苯甲酸或2-氯苯甲酸,E为![]() ,分子式为
,分子式为![]() ;
;
(2) 根据 可知,反应①由A与苯酚发生取代反应生成B和氯化氢,反应类型为取代反应;
可知,反应①由A与苯酚发生取代反应生成B和氯化氢,反应类型为取代反应;
(3)根据![]() →
→ 可知,反应⑥由F与
可知,反应⑥由F与![]() 发生酯化反应生成G和水,反应的化学方程式为
发生酯化反应生成G和水,反应的化学方程式为 ;
;
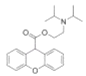
(4)H为 ,含氧官能团的名称是酯基、醚键;
,含氧官能团的名称是酯基、醚键;
(5)N是D(![]() )的同分异构体,含有联苯结构,可与银氨溶液发生银镜反应,则含有醛基,与
)的同分异构体,含有联苯结构,可与银氨溶液发生银镜反应,则含有醛基,与![]() 溶液发生显色反应说明含有酚羟基,则联苯结构上有—OH和-CHO两个取代基,给联苯中碳原子编号
溶液发生显色反应说明含有酚羟基,则联苯结构上有—OH和-CHO两个取代基,给联苯中碳原子编号![]() ,羟基在1位时,醛基有7种取代位置,若羟基在2位时,醛基有7种取代位置,若羟基在3位,醛基有5种取代位置,故符合该条件的D的同分异构体共有19种;其中核磁共振氢谱为六组,峰面积比为1:2:2:2:2:1的结构简式为
,羟基在1位时,醛基有7种取代位置,若羟基在2位时,醛基有7种取代位置,若羟基在3位,醛基有5种取代位置,故符合该条件的D的同分异构体共有19种;其中核磁共振氢谱为六组,峰面积比为1:2:2:2:2:1的结构简式为![]() ;
;
(6)苯乙酸乙酯为合成香料,用于配制各种花香型日用香精。其一种合成路线为: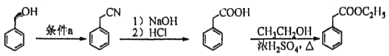 ,根据
,根据![]() 可知,完成转化
可知,完成转化 ,条件a为NaCN、
,条件a为NaCN、![]() ,最后一步反应,乙醇稍过量的目的是使苯乙酸充分反应,提高苯乙酸的转化率。
,最后一步反应,乙醇稍过量的目的是使苯乙酸充分反应,提高苯乙酸的转化率。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A、E在元素周期表中的相对位置如图,A与氧元素能形成两种无色气体,C是地壳中含量最多的元素,D是地壳中含量最多的金属元素。
A | ||
E |
(1)C在元素周期表中的位置为____。
(2)AE2的电子式为___。
(3)C、E、F的单质沸点最低的是__(填化学式)。
(4)C、D、E、F的离子半径由大到小的顺序是___(填离子符号)。
(5)实验室制取F2气体的离子方程式为___。
(6)在微电子工业中,B的最简单气态氢化物的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出以下反应的化学方程式:
(1)Na与水反应:_______
(2)将CO2通入Na2CO3溶液中:_______
(3)将铜粉溶解在浓FeCl3溶液中:_______
(4)向FeCl3溶液中滴加氨水:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁可用于治疗缺铁性贫血。实验室里先制得硫酸亚铁,后将硫酸亚铁与碳酸氢钠反应制得碳酸亚铁(FeSO4+2NaHCO3![]() Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
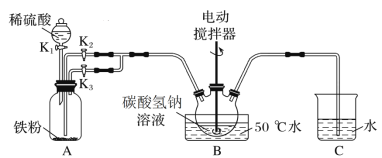
回答下列问题:
(1)A装置中发生反应的化学方程式是________。
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是________。
(3)装置B发生反应生成FeCO3的离子方程式是______。
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为_________。
(5)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是_______。
(6)设计实验检验制得的产品中是否含Fe3+:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙各取300 mL同浓度的盐酸,加入不同质量的同一镁铝合金粉末进行下列实验,有关数据列表如下:
实验序号 | 甲 | 乙 | 丙 |
合金质量/mg | 510 | 765 | 918 |
(标准状况)气体体积/mL | 560 | 672 | 672 |
求:(1)盐酸的物质的量浓度是多少________?
(2)合金中镁铝的质量分数各是多少________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是( )
A.若M甲>M乙,则气体体积:甲<乙
B.若M甲<M乙,则气体的压强:甲>乙
C.若M甲>M乙,则气体的摩尔体积:甲<乙
D.若M甲<M乙,则气体的分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 已知冰的熔化热为6.0kJ·mol-1,冰中氢键键能为20kJmol-1,假设每摩尔冰中有2mol氢键,且熔化热完全用于打破冰的氢键,则最多只能破坏冰中15%的氢键
B. 已知一定温度下,醋酸溶液的物质的量浓度为c,电离度为a,Ka=(ca)2/c(1-a)。若加水稀释,,则CH3COOH![]() CH3COO-+H+向右移动,a增大,Ka不变
CH3COO-+H+向右移动,a增大,Ka不变
C. 甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
D. 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为:MnO2+![]() Zn+(1+
Zn+(1+![]() ) H2O+
) H2O+![]() ZnSO4
ZnSO4![]() MnOOH+
MnOOH+![]() ZnSO4[Zn(OH)2]3·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。
ZnSO4[Zn(OH)2]3·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。
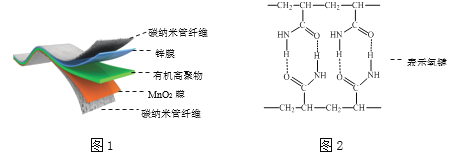
下列说法中,不正确的是( )
A.碳纳米管具有导电性,可用作电极材料
B.合成有机高聚物的单体是:![]()
C.充电时,Zn2+移向Zn膜
D.放电时,电池的正极反应为:MnO2 + e + H+ = MnOOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于电动汽车的铝—空气燃料电池,若以氢氧化钠溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是( )
A.正极反应式为![]()
B.负极反应式为![]()
C.电池在工作过程中电解液的碱性保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com