
【题目】有机物A、B、C有如图所示转化关系: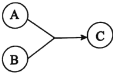 。A的分子式为
。A的分子式为![]() ,A可与
,A可与![]() 的四氯化碳溶液发生加成反应;
的四氯化碳溶液发生加成反应;![]() 能与含
能与含![]() 的溶液恰好完全反应。B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%。试回答下列问题:
的溶液恰好完全反应。B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%。试回答下列问题:
(1)A中所含官能团的名称是_________。
(2)B的分子式为______。B的同系物D的相对分子质量为60,则D可能的结构简式为______。
(3)A与B反应生成C的化学方程式为________,该反应属于_________反应。
【答案】碳碳双键、羧基 ![]()
![]() 、
、![]()
![]() 酯化(或取代)
酯化(或取代)
【解析】
A的分子式为C3H4O2,1molA能与1molNaHCO3溶液恰好完全反应,则A分子含有1个-COOH,A的不饱和度=![]() =2,A可与Br2的四氯化碳溶液发生加成反应,则A分子含有1个C=C双键,故A的结构简式为CH2=CHCOOH;B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%,则B分子中N(C)=
=2,A可与Br2的四氯化碳溶液发生加成反应,则A分子含有1个C=C双键,故A的结构简式为CH2=CHCOOH;B所含元素种类与A相同,相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13%,则B分子中N(C)=![]() =2、N(H)=
=2、N(H)=![]() =6,则N(O)=
=6,则N(O)=![]() =1,故B的分子式为C2H6O,能与A反应生成C,则B含有-OH,故B的结构简式为CH3CH2OH、C为CH2=CHCOOCH2CH3,据此解答。
=1,故B的分子式为C2H6O,能与A反应生成C,则B含有-OH,故B的结构简式为CH3CH2OH、C为CH2=CHCOOCH2CH3,据此解答。
(1)由上述分析可知,A为CH2=CHCOOH,含有碳碳双键、羧基,故答案为:碳碳双键、羧基;
(2)由上述分析可知,B的分子式为C2H6O,结构简式为CH3CH2OH,其同系物D的相对分子质量为60,则相差1个CH2原子团,则D可能的结构简式为CH3CH2CH2OH、![]() ,故答案为:C2H6O;CH3CH2CH2OH、
,故答案为:C2H6O;CH3CH2CH2OH、![]() ;
;
(3)A与B反应生成C的化学方程式为:![]() ,属于酯化反应,故答案为:
,属于酯化反应,故答案为:![]() ;酯化(或取代)。
;酯化(或取代)。


科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在密闭容器反应,达到平衡状态的标志是()
2NO+O2在密闭容器反应,达到平衡状态的标志是()
(1)单位时间内生成n mol O2的同时生成2n mol NO2
(2)单位时间内生成n mol O2的同时生成2n mol NO
(3)用NO2、NO、O2的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态.
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯的结构简式为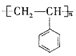 ,试回答下列问题:
,试回答下列问题:
(1)聚苯乙烯的分子式为__________,链节是____________,单体是_________________。
(2)实验测得聚苯乙烯的相对分子质量(平均值)为52000,则该高聚物的聚合度![]() 为________。
为________。
(3)一定条件下合成聚苯乙烯的化学方程式为______,该反应类型为_______反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.用来制造电线电缆的聚乙烯树脂属于热塑性高分子材料
B.研发可降解高分子材料,可以减少“白色污染”
C.棉、麻、羊毛及合成纤维完全燃烧都只生成![]() 和
和![]()
D.硅橡胶![]() 可由
可由![]() 经水解、缩聚两步反应制得
经水解、缩聚两步反应制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃分子中若含有双键、叁键或环,其碳原子所结合的氢原子则少于同碳原子数对应烷烃所含的氢原子数,亦具有一定的不饱和度![]() 用
用![]() 表示
表示![]() 。下表列出几种烃的不饱和度:
。下表列出几种烃的不饱和度:
有机物 | 乙烯 | 乙炔 | 环己烷 | 苯 |
| 1 | 2 | 1 | 4 |
据此下列说法不正确的是![]()
![]()
A.![]() 的不饱和链烃再结合6molH即达到饱和
的不饱和链烃再结合6molH即达到饱和
B.![]() 的
的![]() 等于6
等于6
C.![]() 与环丁烷的不饱和度相同
与环丁烷的不饱和度相同
D.![]() 的不饱和度与
的不饱和度与![]() 、
、![]() 的不饱和度相同
的不饱和度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
(1)将一定量的有机物A置于氧气中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该有机物的实验式是__。
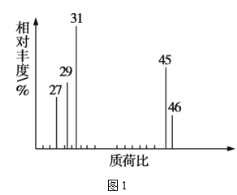
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图1所示的质谱图,则其相对分子质量为___,该物质的分子式是__。
(3)根据价键理论,预测A的可能结构并写出结构简式:___。
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的吸收峰(信号),根据吸收峰(信号)可以确定分子中氢原子的种类和数目。例如氯甲基甲基醚(Cl-CH2-O-CH3,有2种氢原子)的核磁共振氢谱如图2所示:
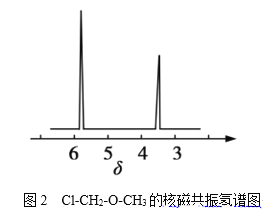
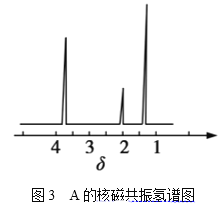
经测定,有机物A的核磁共振氢谱图如图3所示,则A的结构简式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SPC(2Na2CO33H2O2)具有Na2CO3和H2O2的双重性质,广泛应用于印染、医药卫生等领域。以芒硝(Na2SO410H2O)、H2O2等为原料制备SPC的工艺流程如下:
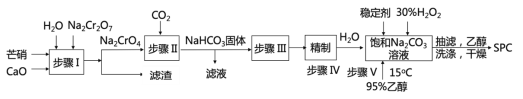
回答下列问题:
(1)步骤I产生的滤渣为__________________(填名称)。
(2)步骤II中发生反应的离子方程式为_________________。其中生成的__________(填化学式)可以循环使用。
(3)步骤V中,合成时需选择温度为15℃,其原因是_____________________。
(4)抽滤后用乙醇洗涤的作用是_______________________________________。
(5)SPC的保存方法是______________________________。
(6)过氧化氢用催化剂催化分解时生成水和氧原子,该氧原子非常活泼,称为活性氧。称量0.1600 g样品,置于250 mL锥形瓶中,并用100 mL 0.5 molL-1硫酸溶解完全,立即用0.02000molL-1KMnO4标准溶液滴定,滴定至终点时溶液颜色为_____,且半分钟内不恢复为原来的颜色,进行三次平行实验,消耗KMnO4溶液的平均体积为26.56 mL。另外,在不加样品的情况下按照上述过程进行空白实验,消耗KMnO4溶液的平均体积为2.24 mL。该样品的活性氧含量为______%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯贝特(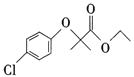 )是临床上一种降脂抗血栓药物,它的一条合成路线如图所示。
)是临床上一种降脂抗血栓药物,它的一条合成路线如图所示。
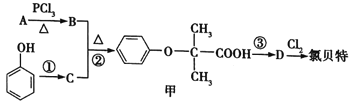
提示:Ⅰ.图中部分反应条件及部分反应物、生成物已略去;
Ⅱ.![]() (
(![]() 代表烃基);
代表烃基);
Ⅲ.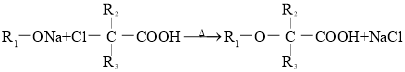 (
(![]() 、
、![]() 、
、![]() 代表烃基)。
代表烃基)。
(1)氯贝特的分子式为_____________________。
(2)A的结构简式为_______________。
(3)要实现反应①所示的转化,加入下列物质不能达到目的的是_________(填选项字母)。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
(4)反应②的反应类型为________________,其产物甲有多种同分异构体,同时满足以下条件的甲的同分异构体有________种(不考虑立体异构)。
①属于1,3,![]() 三取代苯;②属于酯类且既能与
三取代苯;②属于酯类且既能与![]() 溶液反应显色,又能发生银镜反应;③
溶液反应显色,又能发生银镜反应;③![]() 该同分异构体最多能与
该同分异构体最多能与![]() 反应。
反应。
(5)写出B与足量![]() 溶液反应的化学方程式__________________。
溶液反应的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中,可以使0.10mol/LCH3COOH溶液中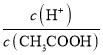 值增大的措施是_______________(填序号)。
值增大的措施是_______________(填序号)。
a.加水稀释b.加入少量CH3COONa固体 c.加入少量冰醋酸d.通入少量HCl气体 e.加少量烧碱溶液 f.升高温度
(2)t℃时,水的离子积常数Kw=1×10-12。
①该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液混合后溶液呈中性,则a+b=_________。
②该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因:_______________________;该混合溶液中:c(A-)-c(Na+)=______________________mol/L(填数值)。
(3)25℃下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。(已知25℃时电离常数:H2CO3 K1=4.4×10-7,K2=4.7×10-11;HClO K=3.0×10-8;CH3COOH K=1.8×10-5)
①三种溶液pH由小到大的顺序为:_______________________________(填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3)_____c(CO32-)(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp(AgCl)=1.8×10-10,现将足量氯化银分别放入:
a.100mL蒸馏水中;
b.100mL0.2mol/LAgNO3溶液中;
c.100mL0.1mol/L氯化铝溶液中;
d.100mL0.1mol/L盐酸溶液中。
充分搅抖后,相同温度下银离子浓度由大到小的顺序是________________(填写序号);b中氯离子的浓度为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com